
科目: 来源: 题型:
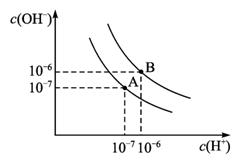
图1-2-13
(1)若A点表示25℃时水的电离平衡状态,当温度升高至100℃时水的电离平衡状态为B点,则此时水的离子积从_________增加到_________。
(2)将100℃ pH=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃恒温,欲使混合液的pH=7,则Ba(OH)2与盐酸的体积比为_________。
(3)向纯水中加入NaHSO4(温度不变)则溶液的_________。
A.pH升高 B.pH降低
C.c(H+)·c(OH-)增大 D.c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
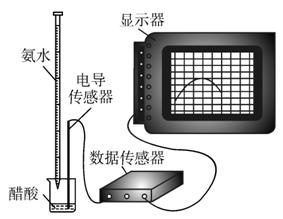
(1)用________(填仪器名称)量取10.00 mL的食用白醋,在________(填仪器名称)中用水稀释后转移到100 mL____________(填仪器名称)中定容,然后将稀释后的溶液倒入试剂瓶中。
(2)量取20.00 mL的上述溶液倒入烧杯中,连接好DIS系统(如上图),向烧杯中滴加浓度为0.100 0 mol/L的氨水,计算机屏幕上显示出溶液导电能力随氨水体积变化的曲线(见图1-2-12)。

图1-2-12
①用滴定管盛氨水前,滴定管要用_______润洗2—3遍,润洗的目的是_________________。
②氨水与醋酸反应的离子方程式是___________________________________________。
③食用白醋中醋酸的物质的量浓度是__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.若x=y,且a+b=14,则pH>7 B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7 D.若x=10 y,且a+b=14,则pH>7
查看答案和解析>>
科目: 来源: 题型:
①用坩埚准确称取2.0 g硫酸铜晶体,记下坩埚和硫酸铜晶体的总质馈m1;
②将盛有硫酸铜品体的坩埚放在三角架上而的泥三角上,缓慢加热,直到蓝色的硫酸铜品体完全变成白色,且不再有水蒸气逸出,然后将坩埚冷却;
③待坩埚冷却后,将坩埚放在天平上称量,记下坩埚和无水硫酸铜的总质量m2。
(1)②中加热硫酸铜晶体时所用的仪器有____________________________________________。
(2)上述每一步实验中,都有一个很关键的步骤没有给出,它们是①______________________;②_________________________;③____________________________。
(3)写出硫酸铜晶体(CuSO4·xH2O)中结晶水的表达式x=_______________________。
(4)该小组最终测定的结果偏高,其原因可能是(选填字母序号)________________________。
A.取出的硫酸铜晶体未研成粉末,就开始加热
B.在①中称量坩埚和硫酸铜晶体时,天平指针偏右
C.加热时,硫酸铜晶体刚变为白色,就停止加热
D.将加热后的白色粉末放在空气中冷却
查看答案和解析>>
科目: 来源: 题型:
A.HN3水溶液中粒子浓度大小顺序为:c(HN3)>c(H+)>c(![]() )>c(OH-)
)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.![]() 与CO2含相等电子数
与CO2含相等电子数
查看答案和解析>>
科目: 来源: 题型:
A.由0.1 mol·L-1的CH3COOH溶液与0.1 mol·L-1的NaOH溶液等体积混合而成
B.由10 mL pH=3的CH3COOH溶液与1 mL pH=11的NaOH溶液混合而成
C.由0.1 mol·L-1的CH3COONa溶液与0.1 mol·L-1的NaOH溶液等体积混合而成
D.由0.1 mol·L-1的CH3COONa溶液与0.1 mol·L-1的CH3COOH溶液等体积混合而成
查看答案和解析>>
科目: 来源: 题型:
A.c(H+)=c(HCl) B.c(H+)=c(HCl)+![]()
C.c(H+)=c(HCl)+Kw D.c(H+)=c(HCl)-![]()
查看答案和解析>>
科目: 来源: 题型:
编号 | HX | YOH | 溶液的体积关系 |
① | 强酸 | 强碱 | V(HX)=V(YOH) |
② | 强酸 | 强碱 | V(HX)<V(YOH) |
③ | 强酸 | 弱碱 | V(HX)=V(YOH) |
④ | 弱酸 | 强碱 | V(HX)=V(YOH) |
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目: 来源: 题型:
A.水的离子积变大、pH变小、呈酸性
B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目: 来源: 题型:
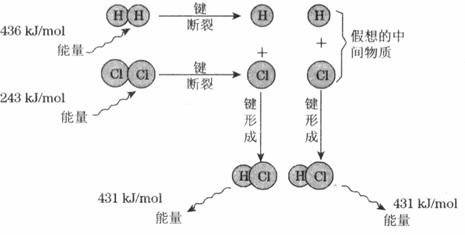
①化学键断裂需要____________(填“释放”或“吸收”)能量;
②图中共释放的能量____________kJ/tool;
③该反应的反应物的总能量___________(填“大于”“等于”或“小于”)反应产物的能量,所以该反应是__________反应;
④用图示数据计算其反应热,写出该反应的热化学方程式
___________________________________________________________________。
(2)已知一个化学方程式可由另外几个化学方程式加减而得到,则该化学反应的能量变化即为这几个化学反应能量变化的代数和。
现有:298 K时
C(s,石墨)+O2(g)====CO2(g);△H1=-393.5 kJ/mol
CO(g)+寺O2(g)====CO2(g);△H3=-283.0 kJ/mol
写出石墨在氧气中反应生成一氧化碳的热化学方程式
_________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com