
科目: 来源: 题型:
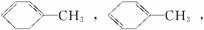 可简写为
可简写为![]()
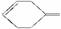
降冰片烯的分子结构可表示为:
(1)降冰片烯属于_____________。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)降冰片烯的分子式为_________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为____________。
(4)降冰片烯不具有的性质___________________________________________。
a.能溶于水 b.能发生氧化反应
c.能发生加成反应 d.常温常压下为气体
查看答案和解析>>
科目: 来源: 题型:
A.2,3,4 B.3,4,5 C.4,5,6 D.5,6,7
查看答案和解析>>
科目: 来源: 题型:
(1)图1-3-31是市场上出售的一种活性炭净水器示意图。这种净水器可以除去水中的难溶性物质,同时利用活性炭的____________作用除去臭味和一些溶解的杂质。

图1-3-31
(2)2003年9月份南京城北污水系统处理一期工程将如期完成,届时湖南路、中山路、新模范马路及下关部分地区的水环境将首先得到改善。为了检测废水是否达到排放标准,请你设计以下实验:
①过滤除去水中的固体杂质,所需的玻璃仪器有___________、___________、___________。
②用___________来检测废水的酸碱度。
(3)三峡工程二期已于2003年6月1日开始蓄水。为防止三峡库区水被污染,应该采取的措施是(填序号) ___________。
①清理蓄水库库底固体废物 ②防治船舶污染 ③整治相关河流污染 ④治理库区和上游区工业污染
(4)许多化学反应都能生成水。请按照以下反应类型,各写一个生成水的化学方程式:____________________________________________
化合反应:_________________________________
分解反应:_________________________________
置换反应:_________________________________
复分解反应:________________________________
(5)载人飞船必须建立水的循环体系,以保证宇航员的生活用水并减少飞船的携水量。请将图1-3-32各项用箭头连接成水的循环体系。(注:氢氧燃料电池反应产生电能,同时生成水)

图1-3-32
查看答案和解析>>
科目: 来源: 题型:
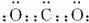
图1-3-29
请回答:
(1)W的电子式是___________________________________。
(2)X与Y在溶液中反应的离子方程式是__________________________________________。
(3)X含有四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用图1-3-30装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
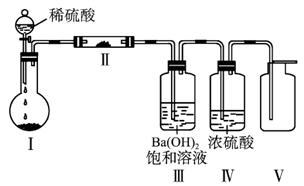
图1-3-30
①装置Ⅰ中反应的化学方程式是 __________________________________________,装置Ⅱ中物质的化学式是___________________________________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是______________,所需仪器装置是_______ (从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是_________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是_______________________。
此液体具有的性质是_________ (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼热后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为_________。
②原无色有刺激性气味的气体与含?1.5 mol? Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是 ___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
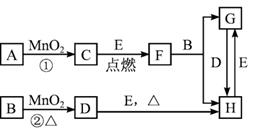
图1-3-27
(1)写出有关物质的名称或化学式:
B__________,F__________,H__________。
(2)指出MnO2在相关反应中的作用:反应①中是__________剂,反应②中是__________剂。
(3)若反应①是在加热条件下进行,则A是__________;若反应①是在常温条件下进行,则A是__________。
(4)写出B与MnO2共热获得D的化学方程式:____________________ 。
查看答案和解析>>
科目: 来源: 题型:
A.BaCl2 NaOH NaHCO3 B.Na2CO3 MgCl2 H2SO4
C.AlCl3 NH3·H2O NaOH D.Ba(OH)2 CaCl2 Na2SO4
查看答案和解析>>
科目: 来源: 题型:
A.晶体硅和晶体碳化硅都是原子晶体
B.碳化硅是一种新型的无机非金属材料
C.制取碳化硅的反应:SiO2+3C![]() SiC+2CO↑中,SiO2是氧化剂,C是还原剂
SiC+2CO↑中,SiO2是氧化剂,C是还原剂
D.碳化硅的熔点比晶体硅高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com