
科目: 来源: 题型:
将等物质的量的两种氧化物溶于100 mL硫酸,而后逐滴加入1.00 mol·L-1的NaOH溶液。当加入的体积V1=50 mL时,开始有沉淀析出,且沉淀量随NaOH的加入量而逐渐增加,当NaOH的体积V2=650 mL时,沉淀量达到最大值,继续滴加NaOH时,沉淀量逐渐减小,当V3=750 mL时,沉淀量不再改变。
(1)最初加入的50 mL NaOH溶液的作用是什么?
(2)计算所用硫酸的浓度。
(3)试判断两种氧化物各是什么,并计算其物质的量。
查看答案和解析>>
科目: 来源: 题型:
2NO2+Na2CO3====NaNO2+NaNO3+CO2↑ ①
NO+NO2+Na2CO3====2NaNO2+CO2↑ ②
(1)根据反应①,每产生22.4 L(标准状况下)CO2,吸收液质量将增加_________g。
(2)配制1 000 g质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O多少克?
(3)现有1 000 g质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4 L(标准状况)CO2时,吸收液质量就增加44 g。
①计算吸收液中NaNO2和NaNO3物质的量之比。
②1 000 g质量分数为21.2%的纯碱在20 ℃经充分吸收硝酸工业尾气后,蒸发掉688 g水,冷却到0 ℃,最多可析出NaNO2多少克?(0 ℃时,NaNO2的溶解度为71.2 g/100 g水)
查看答案和解析>>
科目: 来源: 题型:
(1)通过计算说明干燥后的固体是什么物质。
(2)求原氧化铜的质量。
查看答案和解析>>
科目: 来源: 题型:

图1-5-30
甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性,所以溶液红色褪去。
乙:因为氯气溶于水并与水反应生成HClO,由于HClO的氧化漂白作用而使溶液褪色。
(1)验证甲同学的推测是否正确的方法是;验证乙同学的推测是否正确的方法是_____________________________________________________________________。
(2)如果将NaOH溶液改成酸性KMnO4溶液,把Cl2换成SO2气体,试问用图示所给装置完成喷泉实验是否合理?__________ (填“合理”或“不合理”)。如果认为不合理,请说明你的理由:_____________________________________________________________________。
(3)类似“褪色喷泉实验”还有多种“变色的喷泉实验”。请你按实验要求,分别设计1个“变色喷泉实验”,并填写下列表格:
编号 | 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 |
① | 无色变红色的喷泉 |
| H2O |
|
② | 红色变无色的喷泉 |
|
| SO2 |
(4)有人设计用钠做喷泉实验的装置(如图1-5-31所示,大头钉上是足够量的金属钠),其原理是_______________。实验过程中发现开始时喷出的喷泉压力大,水流急,但随后越来越慢,并且烧瓶不能充满溶液,若钠是足够量的,装置也不漏气,请说明原因:________________
____________________________________________________________________。

图1-5-31
查看答案和解析>>
科目: 来源: 题型:
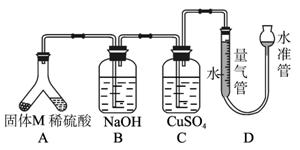
图1-5-29
(1)①固体M中一定有的物质是_____________ (填化学式)
理由是_____________________________________________________________。
②其中一种物质的质量可以确定为__________g(用代数式表示)。
(2)B装置的名称是____________________。
写出B装置中反应的离子方程式________________________________________________。
(3)C装置的作用是______________________________。如果实验中没有B装置,则C装置中产生的现象是______________________________。
(4)稀硫酸和固体M反应后溶液中还残留淡黄色固体,该固体是__________。要分离出该固体。在实验操作中,除烧杯外还需要用到的玻璃仪器是______________________________。
(5)通过进一步实验,测得固体M中各种成分的质量之和小于反应前铁粉和硫粉的质量之和。产生这种现象的原因可能是__________________________________________________。
a.M中有未反应的铁和硫
b.测定气体体积时水准管的水面高于量气管的水面
c.A中留有反应生成的气体
d.气体进入D装置前未用浓硫酸干燥
查看答案和解析>>
科目: 来源: 题型:
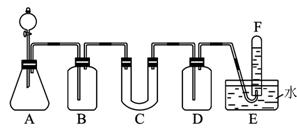
图1-5-28
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用图1-5-28中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:_______________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 |
|
C |
|
|
D |
|
|
(3)写出过氧化钠与二氧化碳反应的化学方程式:___________________________________。
(4)试管F中收集满气体后,下一步实验操作是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.8.4 g B.7.2 g C.3.6 g D.2.1 g
查看答案和解析>>
科目: 来源: 题型:
A.1∶2∶3∶4∶5 B.2∶1∶1∶2∶2
C.1∶1∶4∶3∶5 D.1∶2∶4∶3∶5
查看答案和解析>>
科目: 来源: 题型:

图1-5-27
A.铜与浓硝酸反应制NO2 B.铜与稀硝酸反应制NO
C.乙醇与浓硫酸反应制乙烯 D.氯化钠与浓硫酸反应制HCl
查看答案和解析>>
科目: 来源: 题型:
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有![]()
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有![]()
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有![]()
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com