
科目: 来源: 题型:
制取碳纤维的一种方法是将聚丙烯腈纤维在稀有气体气氛中进行高温处理而获得,这种碳纤维的结构可表示如下:
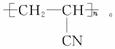
(1)构成这种碳纤维的元素是__________,其原子个数比为__________。
(2)这种碳纤维能否导电?请说明理由。
(3)用乙炔和HCN为原料合成这种碳纤维的流程可表示如下:
![]()
用化学方程式表示以下过程:
①CH≡CH与HCN反应:____________。
②A→B:________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)如果将CO2和H2以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成化学方程式:CO2+4H2![]() _________+2H2O。
_________+2H2O。
(2)若将CO2和H2以1∶3的比例混合,使之发生反应生成某种重要的化工原料和水,则生成的该重要化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(3)已知在443 K—473 K时,用钴(Co)作催化剂可使CO2和H2生成C5—C8的烷烃,这是人工合成汽油的方法之一。要达到该汽油的要求,CO2和H2的体积比的取值范围是V(H2):V(CO2):_________________________________________________________________。
(4)已知在一定条件下,合成尿素的反应为:CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g);ΔH=-127 kJ/mol,在该条件下,将44 g CO2与40 g NH3充分混合,反应放出的热量一定___________(填“大于”“小于”或“等于”)127 kJ。请设计工业合成尿素的条件___________。
CO(NH2)2(s)+H2O(g);ΔH=-127 kJ/mol,在该条件下,将44 g CO2与40 g NH3充分混合,反应放出的热量一定___________(填“大于”“小于”或“等于”)127 kJ。请设计工业合成尿素的条件___________。
查看答案和解析>>
科目: 来源: 题型:
(1)___________________________________________________________________。
(2) __________________________________________________________________。
根据此反应原理,1 mol高氯酸铵分解所产生的气体有__________ mol。
查看答案和解析>>
科目: 来源: 题型:

图1-6-7
(1)左、右储罐中的电解质分别为:左____________,右____________。
(2)写出电池充电时,阳极和阴极的电极反应式。
阳极:________________________________________________,
阴极:________________________________________________。
(3)写出电池充、放电的反应方程式:________________________。
(4)指出在充电过程中钠离子通过膜的流向:________________________。
查看答案和解析>>
科目: 来源: 题型:
已知:①凡与醛基直接相连的碳原子上的氢原子被称为α-H原子,在稀酸或稀碱溶液的催化作用下(最常见的是稀碱溶液催化剂),一分子醛上的α-H原子加成到另一分子醛的氧原子上,其余部分加成到羰基碳原子上生成β-羟基醛,这个反应就叫做羟醛缩合,如
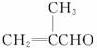
②2R—CH2Cl+2Na![]() R—CH2—CH2—R+2NaCl
R—CH2—CH2—R+2NaCl
合成路线如图1-6-6所示
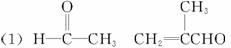
图1-6-6
(1)写出下列物质的结构简式:A___________,D___________。
(2)写出合成路线中有关的反应类型:②___________,⑤___________。
(3)书写有关化学反应方程式:
E→F:______________________;
CH3C(CH3)2Cl→G:___________。
(4)写出C的同分异构体的结构简式(且属于酯类的任意两种):___________、___________。
查看答案和解析>>
科目: 来源: 题型:
(1)写出将绿色植物的秸秆转化为乙醇的化学方程式:________________________________。
(2)已知:C2H5OH(l)+3O2(g)![]() 2CO2(g)+3H2O(l);ΔH=-1 367 kJ·mol-1
2CO2(g)+3H2O(l);ΔH=-1 367 kJ·mol-1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1
CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1
若某种植物的秸秆含纤维素约50%,由植物秸秆经过一系列转化得到乙醇原料的总利用率为80%,则用1 000 g秸秆为原料制得的乙醇燃料燃烧所产生的热量与________L(标准状况下)甲烷完全燃烧产生的热量相当。
(3)绿色植物光合作用的效能是________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)将如图方框中的反应填补完整:
H吸附 ;O吸附 。
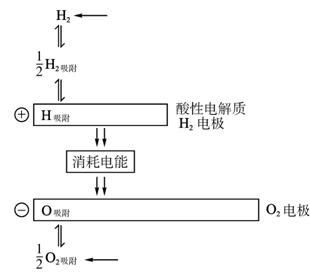
图1-6-5
(2)该电池反应为______________________________。
(3)人们将它用于航天飞行器上原因有两个:一是____________________,因此减轻质量就等于降低向太空发射的费用,与另一种绿色能源__________配合,可以使飞行器在空间停留的时间较长;二是______________________________,更可减少携带重量。
查看答案和解析>>
科目: 来源: 题型:
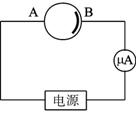
图1-6-4
制造太阳能电池需要高纯度的硅,工业上由粗硅制高纯度硅常通过以下反应实现:
①Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g);ΔH=-381 kJ
SiHCl3(g)+H2(g);ΔH=-381 kJ
②SiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)
Si(s)+3HCl(g)
(1)元素硅在周期表中位于__________;晶体硅属于__________晶体,是__________ (填“导体”“半导体”或“绝缘体”);晶体硅有类似金刚石的结构,每摩尔晶体硅的共价键数目为____________________,键角为__________。
(2)关于上述条件下的两个反应的叙述不正确的是( )
A.两个反应都是置换反应 B.反应②是放热反应
C.上述反应是可逆反应 D.两个反应都是氧化还原反应
(3)反应②的热效应为____________________。
查看答案和解析>>
科目: 来源: 题型:
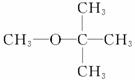
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH3OC(CH3)3来生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间连接形式是________。
(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要的成分是__________。能说明它是正四面体而非正方形平面结构的理由是__________
①其一氯取代物不存在同分异构体
②其二氯取代物不存在同分异构体
③它是非极性分子
④它的键长和键角都相等
(3)1980年我国首次制成一辆燃氢汽车,乘员12个,以50 km/h行驶了40 km。为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又经济的制氢方法是__________
①电解水 ②锌和稀硫酸反应 ③光解海水
查看答案和解析>>
科目: 来源: 题型:
A.可燃冰是在低温、高压下形成的
B.可燃冰晶体属于分子晶体
C.可燃冰属于可再生能源
D.可燃冰开采不当可引起地质灾害和温室效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com