
科目: 来源: 题型:

A.维生素C的化学式为C6H8O6 B.维生素C可作食品添加剂
C.维生素C可发生水解反应 D.维生素C不可能发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
A.蛋白质在紫外线的照射下会失去生理活性
B.蛋白质溶液不能发生丁达尔效应
C.溶液中加入CuSO4可产生盐析现象
D.蚕丝、羊毛、棉花的主要成分都是蛋白质
查看答案和解析>>
科目: 来源: 题型:
A.白磷是红磷的同素异形体,它们有相同的物理性质和化学性质
B.农村及城市生活污水含磷元素,排入江河易引起水体富营养化,造成藻类过分繁殖,影响水质
C.少量白磷通常保存在CS2中
D.实验室未用完的白磷应弃入废液缸中
查看答案和解析>>
科目: 来源: 题型:
A.通入氯化氢 B.加少量氢氧化钠固体
C.加水 D.升温
查看答案和解析>>
科目: 来源: 题型:
①2H2S+SO2====3S↓+2H2O
②S+2H2SO4(浓)====3SO2↑+2H2O
③3S+6KOH====2K2S+K2SO3+3H2O
A.反应①说明SO2能与酸反应,具有碱性氧化物的性质
B.反应②改用稀H2SO4,则能放出H2
C.反应②和③说明S具有两性元素的性质
D.反应③说明S既有氧化性又有还原性
查看答案和解析>>
科目: 来源: 题型:
A.浓硝酸在光照下变黄,说明浓硝酸不稳定,且产物有红棕色气体且可溶于浓硝酸
B.向某溶液中加入氯化钡溶液和稀硝酸,有白色沉淀生成,说明该溶液中一定含有![]()
C.常温下,将铜放入浓硫酸中无明显变化,说明铜在冷、浓硫酸中钝化
D.氯气使湿润的碘化钾淀粉试纸变蓝,说明氯气与淀粉反应
查看答案和解析>>
科目: 来源: 题型:
A.用稀盐酸处理试管中的FeS固体
B.用乙醇浸泡试管中少量的苯酚
C.用硝酸处理试管中的“银镜”
D.将Fe(NO3)2和稀硫酸同时倒入废液缸
查看答案和解析>>
科目: 来源: 题型:
A.KMnO4酸性溶液 B.H2O2
C.NaClO D.NH3·H2O
查看答案和解析>>
科目: 来源: 题型:
(1)写出Cu2O跟稀硝酸反应的化学方程式。
(2)产物中硝酸铜的物质的量。
(3)如混合物中含0.01 mol Cu,则其中Cu2O、CuO的物质的量分别为多少?
(4)如混合物中Cu的物质的量为x,求其中Cu2O、CuO的物质的量及x的取值范围。
查看答案和解析>>
科目: 来源: 题型:
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气,放出热量624 kJ(25℃时),N2H4完全燃烧反应的热化学方程式是____________________________________________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质是20%—30%的KOH溶液。写出肼-空气燃料电池放电时正、负极的电极反应式。
正极:________________________________,
负极:________________________________
(3)图2-2-5是一个电化学过程示意图。
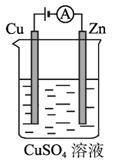
图2-2-5
①锌片上发生的电极反应是________________________________________________。
②假设使用肼?空气燃料电池作为本过程中的电源、铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标标准状况下的空气___________L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com