
科目: 来源: 题型:
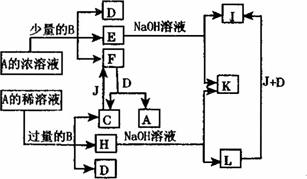
请回答:
(1)常温下B在A的浓溶液中难以反应而溶解的原因是________________________________。
(2)写出下列化学方程式:
F→C+A:_________________________________________________________;
过量B与A的稀溶液反应的离子方程式:___________________________________________;
E→I的离子方程式:____________________________________________________。
(3)L转变为Ⅰ的现象是____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 工业生产硫酸用水吸收SO3 | SO3可与水反应 | Ⅰ对;Ⅱ对;有 |
B | Cl2和SO2混合后可用于漂白纸浆 | Cl2和SO2都有较好的漂白作用 | Ⅰ对;Ⅱ错;无 |
C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的光 | Ⅰ对;Ⅱ对;无 |
D | 石墨常用作电解池的电极 | 石墨的化学性质稳定且导电性好 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
科目: 来源: 题型:
完成下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为____________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式______________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是____________________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水
③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐和氨水反应的离子方程式____________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因__________________。
查看答案和解析>>
科目: 来源: 题型:

(1)Ti的原子序数为22,Ti位于元素周期表中第_________周期,第_________族。
(2)步骤①加Fe的目的是:______________________________________________;
步骤②冷却的目的是:__________________________________________________。
(3)上述制备TiO2的过程中,可以利用的副产物是____________;考虑成本和废物综合利用因素,废液中应加入____________处理。
(4)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
TiO2![]() TiCl4
TiCl4![]() Ti
Ti
已知:①C(s)+O2(g)====CO2(g);ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g) ====2CO2(g);ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) ====TiCl4(s)+O2(g);ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s) ====TiCl4(s)+2CO(g)的ΔH=____________。
反应TiCl4+2Mg====2MgCl2+Ti在Ar环境中进行的理由是______________________。
查看答案和解析>>
科目: 来源: 题型:
(1)C和D反应生成的化合物的电子式是____________。
(2)上述②中化合物的热稳定性____________强于____________(填化学式)。
(3)将D通入B、C生成的化合物中,发生反应的化学方程式是____________________。
(4)A、C、D所含元素可组成一种离子化合物,该化合物发生水解反应的离子方程式是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
查看答案和解析>>
科目: 来源: 题型:
A.黄铁矿煅烧:2FeS2+5O2![]() 2FeO+4SO2
2FeO+4SO2
B.石英与石灰石共熔:SiO2+CaO![]() CaSiO3
CaSiO3
C.氨的催化氧化:4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
D.氯气与石灰乳反应:2Cl2+2Ca(OH)2====CaCl2+CaClO3+2H2O
查看答案和解析>>
科目: 来源: 题型:
A.1.2 mol B.1.5 mol C.1.8 mol D.2.5 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com