
科目: 来源: 题型:
序号 | 实验操作 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
C | 测定Na2CO3、Na2SO4两溶液的pH | 比较碳、硫的非金属性强弱 |
D | 用同一电路测定等浓度的盐酸、醋酸溶液的导电性 | 比较盐酸、醋酸的酸性强弱 |
查看答案和解析>>
科目: 来源: 题型:

(1)如果选用测定反应物CuO和生成物H2O的质量m(CuO)、m(H2O)时,请用上图所示的仪器设计一个简单的实验方案。
①仪器连接的顺序(填编号,仪器可重复使用)是___________________;D中浓硫酸的作用是___________________________________________________;实验完毕时,观察到A中的现象是______________________________________________________________。
②列出计算Cu的相对原子质量的表达式___________________________________________。
③下列情况将使测定结果偏大的是_______________。
a.CuO未全部还原为Cu; b.CuO受潮; c.CuO中混有Cu
(2)如果仍采用上图所示的仪器装置,设计其他方案,还可测定的物理量有_____________。
A.m(Cu)和m(CuO) B.m(N2)和m(H2O)
C.m(Cu)和m(H2O) D.m(NH3)和m(H2O)
查看答案和解析>>
科目: 来源: 题型:阅读理解
某研究性学习小组设计用如下方法测定某居室空气中甲醛的含量(假设空气中无其他还原性气体):
Ⅰ.测定原理:KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸,其反应的离子方程式为:
4![]() +5HCHO+12H+====4Mn2++5CO2↑+11H2O
+5HCHO+12H+====4Mn2++5CO2↑+11H2O
2![]() +5H2C2O4+6H+====2Mn2++10CO2↑+8H2O
+5H2C2O4+6H+====2Mn2++10CO2↑+8H2O
Ⅱ.测定装置:部分装置如下图所示(a、b为止水夹)

Ⅲ.实验步骤:
①检查装置气密性(气密性良好)。
②用A仪器准确移取25.00 mL 1.00×10-3 mol·L-1的高锰酸钾溶液(过量)于广口瓶中并滴入3滴6 mol·L-1 H2SO4溶液备用。
③将2.00×10-3 mol·L-1的草酸标准溶液置于A仪器中备用。
④打开a,关闭b,用注射器抽取100 mL新装修的室内空气。关闭a,打开b,再缓缓推动注射器,将气体全部推入高锰酸钾酸性溶液中,使其充分反应。再如此重复4次(共5次)。
⑤将广口瓶中的溶液转入锥形瓶中(润洗广口瓶2—3次,并将洗涤液全部转入锥形瓶)。
⑥用标准草酸溶液滴定锥形瓶中的溶液,记录滴定所消耗的草酸溶液体积。
⑦再重复实验2次。
Ⅳ.数据处理:分别于装修完工后的第1天、第7天、第30天(室内始终保持通风换气状况)对室内空气进行取样,通过实验测得以下三组数据(每次实验所取的KMnO4溶液均为25.00 mL):
装修后第n天 | 草酸溶液/mL | 甲醛的浓度/mg·m-3 | |||
1 | 2 | 3 | 平均值 | ||
1 | 15.86 | 15.72 | 15.67 | 15.75 |
|
7 | 26.24 | 26.36 | 26.31 | 26.30 |
|
30 | 30.90 | 30.67 | 30.81 | 30.79 |
|
请完成下列问题:
(1)A仪器名称是_________________ 。
(2)步骤④如果压送气体时速度过快,可能会产生什么不利后果?
_____________________________________________________________________。
(3)步骤⑤如果没有润洗,所测甲醛的含量将____________(填“偏高”“偏低”或“无影响”)。
(4)本实验是否需要指示剂(如果需要,请写出指示剂的名称;如果不需要,试说明终点时的实验现象):___________________________________________________________________。
(5)假设KMnO4溶液的物质的量浓度为c1 mol·L-1,所取KMnO4溶液的体积为V1 mL;草酸溶液的物质的量浓度为c2 mol·L-1,消耗草酸溶液的平均体积为V2 mL。
则:计算室内空气中甲醛浓度(mg·m-3)的代数式为____________,第30天室内空气中甲醛浓度为____________,并判断此时主人____________(填“能”或“否”)入住。
查看答案和解析>>
科目: 来源: 题型:
A.新制的硫酸亚铁溶液和过氧化氢溶液反应:2Fe2++2H++H2O2====2Fe3++2H2O
B.向明矾KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至![]() 恰好沉淀完全:
恰好沉淀完全:
2Al3++3![]() +3Ba2++6OH-====2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-====2Al(OH)3↓+3BaSO4↓
C.向次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O====CaSO3↓+2HClO
D.碳酸氢铵溶液与足量氢氧化钠溶液反应:![]() +OH-====NH3·H2O
+OH-====NH3·H2O
查看答案和解析>>
科目: 来源: 题型:
四种盐在不同温度下的溶解度(g/100 g水)表
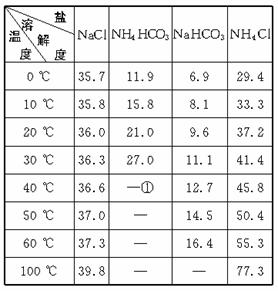
①>35 ℃ NH4HCO3会有分解
请完成下列问题:
(1)反应温度控制在30 ℃—35 ℃,是因为若高于35 ℃,则_______________________,若低于30 ℃,则______________________________________;为控制此温度范围,采取的加热方法为___________________________________。
(2)加料完毕后,继续保温30分钟,目的是________________________________ 。静置后只析出NaHCO3晶体的原因是_____________________________。用蒸馏水洗涤NaHCO3晶体的目的是除去________________________________杂质(以化学式表示)。
(3)过滤所得的母液中含有_______________________(以化学式表示),需加入______________________,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1—2滴酚酞指示剂,用物质的量浓度为c( mol·L-1)的HCl溶液滴定至溶液由红色到无色(指示![]() +H+====
+H+====![]() 反应的终点),所用HCl溶液体积为V1 mL,再加1—2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液总体积为V2 mL。写出纯碱样品中NaHCO3质量分数的计算式:
反应的终点),所用HCl溶液体积为V1 mL,再加1—2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液总体积为V2 mL。写出纯碱样品中NaHCO3质量分数的计算式:
w(NaHCO3)= __________________。
查看答案和解析>>
科目: 来源: 题型:
实验用品:
仪器:电子天平、砂纸、水槽、100 mL烧杯、铁架台、单孔橡皮塞(玻璃管上带橡胶管和止水夹)、铜丝、30 mL酸式滴定管、100 mL小口径测气管(见下图)。
![]()
药品:镁条、水、15 mol·L-1的浓硫酸。
(1)本实验用0.6 mol·L-1的硫酸进行反应,活动小组共需要480 mL该浓度的硫酸,写出用15 mol·L-1的浓硫酸配制0.6 mol·L-1的硫酸时,还用到的仪器名称和规格____________、____________、____________;需要15 mol·L-1的浓硫酸____________mL。
(2)选用上述仪器的药品进行实验,补写下列实验步骤:
①取一段镁条,擦去氧化膜,称量;
②用细铜丝包裹镁条,铜丝的另一端插在单孔橡皮塞(玻璃管上带橡胶管和止水夹)上;
③_____________________________________________________________;
④_____________________________________________________________;
⑤_____________________________________________________________;
⑥待镁条全部反应后,放置一段时间,调节测气管中水面高度,使管中水面与水槽中水面相平,读出氢气体积。
(3)问题讨论:
①在标准状况下,其他操作都正常,为了保证实验成功,取用的镁条质量应小于_________________g,所用的稀硫酸应大于_________________mL。
②在标准状况下,某学生进行了5次实验,将实验数据通过计算,结果如下:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
H2的体积(L·mol-1) | 23.45 | 22.41 | 22.38 | 22.39 | 22.42 |
则通过实验验证,标准状况下,1 mol H2的体积为____________L。
查看答案和解析>>
科目: 来源: 题型:
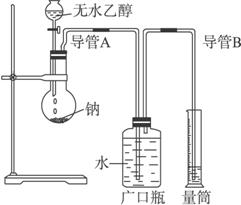
(1)指出实验装置中的错误____________。
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将____________(填“偏大”“偏小”或“不变”)。
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知在酸性溶液中,碘酸钾和亚硫酸钠会发生如下一些反应:
①![]() +3
+3![]() ====3
====3![]() +3H++I-(慢)
+3H++I-(慢)
②![]() +5I-+6H+====3I2+3H2O(慢)
+5I-+6H+====3I2+3H2O(慢)
③I2+![]() +H2O====2I-+
+H2O====2I-+![]() +3H+(快)
+3H+(快)
分别配制下面三种溶液。
溶液A:0.9 g碘酸钾溶于少量温水中,再稀释到500 mL。
溶液B:0.45 g亚硫酸钠配成溶液,稀释到500 mL。
溶液C:取5 g可溶性淀粉,放在小烧杯中,加入25 mL冷水,搅拌成悬浊液。另取200 mL水加热至沸,趁沸腾时倒入淀粉悬浊液并迅速搅拌,使淀粉糊化、溶解。到溶液冷却后边搅拌边慢慢加入12.5 mL浓硫酸,最后也稀释到500 mL。
溶液D:200 mL水+50 mL A液+500 mL C液
溶液E:225 mL水+25 mL A液+50 mL C液
试完成下列问题:
(1)根据实验原理,化学反应速率由哪步反应决定____________。(填“①”“②”或“③”)
(2)当哪种离子耗尽时才能见到溶液变蓝色____________。(填“I-”“![]() ”“H+”或“
”“H+”或“![]() ”)
”)
(3)在盛放D液和E液的两只烧杯里同时加入50 mL B液。D、E两烧杯哪个溶液先变蓝色____________(填“D”或“E”)
(4)为研究温度对反应速率的影响,准备三份E液(各300 mL,配法同上),用三只量筒分别量取50 mL B液,同时把三份B液分别加入下述不同温度的三份E液中。
a.第一份放在石棉网上加热到50 ℃左右,b.第二份维持在室温,c.第三份浸在冰水里冷却到近冰点。先变蓝色的是____________。(填“a”“b”或“c”)
查看答案和解析>>
科目: 来源: 题型:
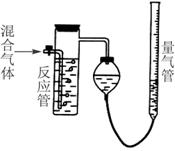
反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O====H2SO4+2HI
(1)混合气体进入反应管后,量气管内增加的水的体积等于____________的体积(填写气体的化学式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量____________(填“偏高”“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为c mol·L-1,N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积分数为____________ 。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为____________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
科目: 来源: 题型:
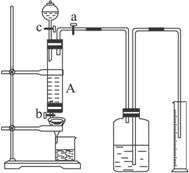
完成下列问题:
(1)如何检查装置A的气密性:__________________。
(2)实验时打开a,关闭b,从分液漏斗内向A中加过量的稀盐酸,观察到的现象是__________________________;滴加盐酸时,发现反应速率较相同浓度盐酸与铁粉反应要快,其原因是________________________________________________________________。
(3)待A中的物质反应完成后,打开b,进行过滤,滤液过滤到盛有过氧化氢的烧杯中,发生反应的化学方程式为:________________________________。
(4)要从烧杯内溶液得到FeCl3·6H2O晶体,主要操作包括:_________________________________________________。
(5)实验室若没有过氧化氢,可用下列 _________试剂代替(填选项)。
A.过量稀硝酸 B.过量氯水 C.过量氨水 D.过量氢氧化钠溶液
(6)若要测废铁屑中铁的纯度,测出放出气体的体积V(已折算成标准状况,单位:L),则废铁屑的纯度为 _________(用m、V的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com