
科目: 来源: 题型:
A.3.56 mol·L-1 B.5.23 mol·L-1 C.4.33 mol·L-1 D.5.00 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
A.该温度下NaNO3的溶解度为100 g
B.原不饱和溶液中NaNO3质量分数为![]() %
%
C.原不饱和溶液中NaNO3物质的量浓度为![]() mol·L-1
mol·L-1
D.原不饱和溶液的密度为![]() g·mL-1
g·mL-1
查看答案和解析>>
科目: 来源: 题型:
A.室内使用煤炉取暖时,为防止煤气中毒应确保煤充分燃烧和烟道通畅
B.氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域
C.家中发生天然气泄露时,应立即使用室内电话报警
D.漂白粉与浓盐酸不能混合使用,否则易产生有毒气体
查看答案和解析>>
科目: 来源: 题型:
已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是_____________。
(2)Z2Y2与X2Y反应的化学方程式是__________________________。
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
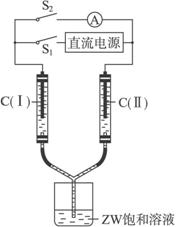
接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时:
C(I)的电极名称是_____________(填写“正极”或“负极”);
C(II)的电极反应式是_____________。
(4)铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入Z2Y2,铜屑可逐渐溶解,该反应的离子方程式是______________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)此时溶液的溶质如果是单一成分,可能是____________,如果是多种成分,可能是____________。
(2)在上述所得的溶液中,逐滴缓慢滴加盐酸 1 mol·L-1,所得气体(不考虑溶解于水)的体积与所加的盐酸的体积关系如下图所示:
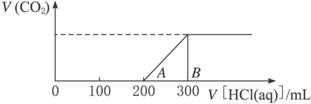
①加入200 mL 盐酸之前,无气体产生,写出A点之前发生反应的离子方程式___________________________________。
②求产生的二氧化碳在标准状况下的体积多少。
③求B点时,反应所得溶液中溶质的物质的量浓度是多少。(溶液体积的变化忽略不计)。
查看答案和解析>>
科目: 来源: 题型:
(1)当生成沉淀的质量刚好最大时,消耗CO2的体积224 mL(标准状况)。在下图所示的坐标系中,画出生成沉淀的质量(m)与通入CO2的体积(V)的关系图。图中,生成沉淀的最大质量为_____________g,沉淀刚好全部溶解时消耗CO2的体积为_____________mL,混合物中KOH的质量为_____________g。
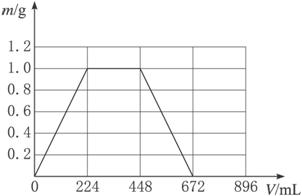
(2)若KOH和Ca(OH)2以任何比例混合,总质量仍保持1.3 g不变,则消耗CO2的总体积 V 的取值范围为___________mL<V<___________mL。
查看答案和解析>>
科目: 来源: 题型:
物质 | A | B | CO | H2 |
燃烧热/kJ·mol-1 | 725 | 5 518 | 283 | 286 |
A、B按不同比例混合的燃料有91.2 g,在足量的O2中燃烧时,放出的热量Q与B的物质的量分数x的关系如下图所示。
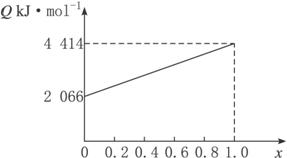
(1)求A、B的相对分子质量。
(2)等物质的量A、B混合的燃料有73 g,在160 L O2中完全燃烧,得到104 L气体,通过碱石灰吸收后剩余3.2 L(气体体积均在标准状况下测定)。由此可推得混合物中原子个数比N(C)∶N(H)∶N(O)是多少?写出A和B的化学式。
(3)求1 mol由A、B等物质的量混合而成的燃料在一定的氧气中燃烧,放出2 980 kJ的热量,则反应中生成CO的物质的量。
查看答案和解析>>
科目: 来源: 题型:

(1)若用2.49 g样品进行同样的实验时,产生CO2___________mL(标准状况)。
(2)另取3.32 g天然碱样品于300 ℃加热分解至完全(300 ℃ 时 Na2CO3不分解),产生CO2 112 mL(标准状况)和水0.45 g,试通过计算确定该天然碱的化学式。
(3)所用盐酸的物质的量浓度为______________________。
(4)若在上述某次实验中,收集到336 mL(标准状况)气体,该次实验中称取天然碱样品的质量可能是______________________。
查看答案和解析>>
科目: 来源: 题型:
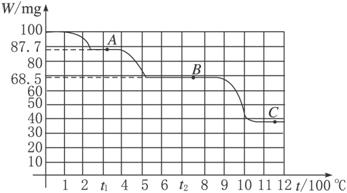
(1)温度分别为t1和t2时,固体产物的化学式A是______________,B是________________。
(2)由CaC2O4·H2O得到A的化学方程式为_______________________________________。
(3)由A得到B的化学方程式为___________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0。当反应进行到时间t0时达到平衡状态,测得混合气体的总物质的量为2.1 mol。试回答:
2SO3(g);ΔH<0。当反应进行到时间t0时达到平衡状态,测得混合气体的总物质的量为2.1 mol。试回答:
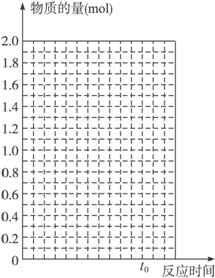
(1)在上图中作出反应混合物中各组分气体的物质的量随反应进行到t0时的变化曲线。
(2)当反应进行到t1时间时(t1 >t0),给上述反应容器加热到温度为T2(T2>T1),反应在t3时间时(t3>t1)重新达到平衡状态,新平衡混合物中气体的总物质的量________2.1 mol(填“<”“>”或“=”)。
(3)若起始时加入0.6 mol SO2、0.3 mol O2和x mol SO3,保持温度不变,达到平衡状态后,各气体的体积分数与上述平衡状态相同,x的值为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com