
科目: 来源: 题型:
(1)用金属镁将水体中的![]() 还原为N2,从而消除污染,其反应的离子方程式是:
还原为N2,从而消除污染,其反应的离子方程式是:
2![]() +5Mg+6H2O====N2↑+5Mg(OH)2+2OH-。金属镁是从海水中提取MgCl2,然后再通过电解制得。若要除去1 m3含0.3 mol氮元素的废水中的
+5Mg+6H2O====N2↑+5Mg(OH)2+2OH-。金属镁是从海水中提取MgCl2,然后再通过电解制得。若要除去1 m3含0.3 mol氮元素的废水中的![]() ,则至少需要含0.5%(质量分数)MgCl2的海水多少千克?
,则至少需要含0.5%(质量分数)MgCl2的海水多少千克?
(2)把甲醇加入含![]() 的废水中也可消除氮的污染,在微生物作用下
的废水中也可消除氮的污染,在微生物作用下![]() 和CH3OH均转化为无毒气体和水,请写出该反应的离子方程式。若某废水用上述方法处理时,
和CH3OH均转化为无毒气体和水,请写出该反应的离子方程式。若某废水用上述方法处理时,![]()
![]() N2的转化率为a%,那么每天处理含
N2的转化率为a%,那么每天处理含![]() 为b g·L-1的废水V m3(密度1 g·cm-3),需要甲醇多少千克?(要求写出解题步骤,运算过程中的数据及最后结果可写出运算式,可以不化简)
为b g·L-1的废水V m3(密度1 g·cm-3),需要甲醇多少千克?(要求写出解题步骤,运算过程中的数据及最后结果可写出运算式,可以不化简)
查看答案和解析>>
科目: 来源: 题型:
(1)若原有机物在标准状况下是单一气体,通过计算推断它的分子式。
(2)若原物质是按等物质的量混合的两种有机化合物,请写出它们的结构简式(至少写两组)。
查看答案和解析>>
科目: 来源: 题型:
①将2.000 L的气体样品通过盛有I2O5固体的加热管,发生的反应为:
5CO+I2O5![]() 5CO2+I2。
5CO2+I2。
②将所产生的碘升华,并加入30.00 mL 0.005 0 mol·L-1的硫代硫酸钠溶液,发生的反应为:
I2+2![]() ====2I-+
====2I-+![]()
③将②中溶液取出![]() ,加入1.000 mL 0.010 0 mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
,加入1.000 mL 0.010 0 mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
试计算1 L该气体样品中有多少毫克的CO?
查看答案和解析>>
科目: 来源: 题型:
A.pH=2和pH=1的溶液中c(H+)之比为1∶10
B.Na2CO3溶液中c(Na+)与c(![]() )之比为2∶1
)之比为2∶1
C.0.2 mol·L-1与0.1 mol·L-1醋酸溶液中c(H+)之比为2∶1
D.NO2溶于水时,被氧化的与被还原的n(NO2)之比为3∶1
查看答案和解析>>
科目: 来源: 题型:
A.降低平衡体系的温度,逆反应速率变小,正反应速率增大,平衡正向移动
B.恒温下达到平衡的标志是C和D的生成速率相等
C.A的平均反应速率为0.15 mol·(L·min)-1
D.B的转化率为25%
查看答案和解析>>
科目: 来源: 题型:
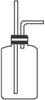
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在答题卡上相应图中把导管补充完整。
(2)实验中他们取
①请写出铜跟浓硫酸反应的化学方程式:_____________________。
②为什么有一定量的余酸但未能使铜片完全溶解?你认为原因是:____________________。
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:_________(填写字母编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)请设计一个可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)。
查看答案和解析>>
科目: 来源: 题型:
A.二糖 B.多糖
C.氨基酸 D.脂肪
查看答案和解析>>
科目: 来源: 题型:
N2(g)+2O2(g)====2NO2(g);ΔH=67.7 kJ·mol-1
N2H4(g)+O2(g) ====N2(g)+2H2O(g);ΔH=-534 kJ·mol-1
则下列N2H4和NO2反应的有关说法不正确的是( )
A.燃烧时NO2作氧化剂
B.氮气既是氧化产物又是还原产物
C.生成1 mol N2转移8 mol e-
D.该反应的热化学方程式为2N2H4(g)+2NO2(g) ====3N2(g)+4H2O(g);ΔH=-1135.7 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.![]() mol·L-1 B.
mol·L-1 B.![]() mol·L-1 C.
mol·L-1 C.![]() 2mol·L-1 D.
2mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目: 来源: 题型:
A.1∶2∶3 B.3∶2∶1 C.6∶3∶1 D.6∶3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com