
科目: 来源: 题型:

(1)物质X的化学式是_______________。
(2)化合物B中所包含的化学键有_____________和_____________。
(3)反应④的离子方程式为______________。反应②的化学方程式为______________,其中还原剂是_____________。
(4)已知每生成16 g E,放出106.5 kJ的热量,则反应①的热化学反应方程式为____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
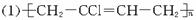
(1)写出D的结构简式_______________________________________________。
(2)写出B的结构简式_____________________________________________。
(3)写出第②步反应的化学方程式____________________________________________。
(4)写出富马酸的一种相邻同系物的结构简式_____________________________________。
(5)写出第⑨步反应的化学方程式_____________________________________________。
(6)以上反应中属于消去反应的是____________(填入编号)。
查看答案和解析>>
科目: 来源: 题型:
①A+B![]() M+D+E;②M+E
M+D+E;②M+E![]() A+F+B。请针对以下两种不同情况完成下列问题:
A+F+B。请针对以下两种不同情况完成下列问题:
(1)若A是一种日常生活中用作调味剂的盐,反应①是化学工业上制取单质E和化合物M的重要方法。则A的电子式为________________;反应②的离子方程式为________________;在酸性条件下,若将化合物F加到含Fe2+的溶液中,溶液从浅绿色变成黄色,该反应的离子方程式为________________________________________________。
(2)若A是一种含氧酸盐,可用于实验室中检验水的存在。1个A的酸根离子中共含有50个电子,其中含有一种元素X,X的原子最外层电子数是电子层数的2倍,则X在元素周期表中的位置是________________。X单质的熔点是112.8 ℃,则X单质的晶体类型属于________________晶体。以石黑作电极电解A溶液,电流强度为a A,时间t min 后阴极增重w g,在阳极得V L纯净气体,则阿伏加德罗常数NA的计算式是(1个电子的电荷量为q C)_________________________。
查看答案和解析>>
科目: 来源: 题型:
A.只有①② B.只有②⑤ C.只有①⑤ D.只有②④⑤
查看答案和解析>>
科目: 来源: 题型:
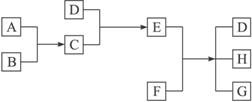
(1)D的化学式(分子式)是____________。E的化学式(分子式)是___________________。
(2)A和B反应生成C的化学方程式是___________________________________________。
(3)E和F反应生成D、H和G的化学方程式是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
![]()
请完成下列问题:
(1)W的电子式是________________________。
(2)X与Y在溶液中反应的离子方程式是_________________________________________。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。

①装置Ⅰ中反应的化学方程式是________________________________________________,
装置Ⅱ中物质的化学式是__________________________________________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体,该化合物的化学式是_____________所需仪器装置是_______________________(从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
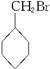
6-羰基庚酸是合成某些高分子材料和药物的重要中间体。某实验室以溴代甲基环己烷为原料合成6-羰基庚酸,请用合成反应流程图表示出最合理的合成方案(注明反应条件)。
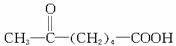
溴代甲基环己烷(也可以表示为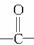 )
)
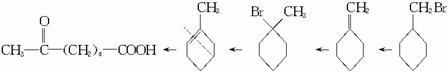
6-羰基庚酸
提示:①合成过程中无机试剂任选;
②合成反应流程图表示方法示例如下:
![]()
查看答案和解析>>
科目: 来源: 题型:
(1)Y、Z、W的原子半径由小到大的顺序是______________________________________。
(2)ZW2的电子式是_________,它在常温下呈液态,形成晶体时,属于__________晶体。
(3)工业生产单质Y的原理是______________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是______________。
(5)0.1 mol的单质W与50 mL 1.5 mol·L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是________________。
查看答案和解析>>
科目: 来源: 题型:
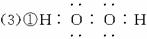
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请完成下列问题:
(1)红褐色胶体中F粒子直径大小的范围:__________________________________________。
(2)A、B、H的化学式:A______________、B______________、H______________。
(3)①H2O2分子的电子式:____________________________________________。
②写出C的酸性溶液与双氧水反应的离子方程式:___________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:______________________________________。
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:__________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
元素编号元素性质 | ① | ② | ③ | ④ | ⑤ |
原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 |
最高价态 | +1 | +1 | — | +3 | +4 |
最低价态 | — | — | -2 | — | -4 |
元素编号元素性质 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
原子半径(10-10m) | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
最高价态 | +5 | +7 | +1 | +5 | — |
最低价态 | -3 | -1 | — | -3 | -1 |
试完成下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是_________(填写编号)。
(2)上述⑤⑥⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)____________________________。某元素R的原子半径为1.02×10-10 m,该元素在周期表中位于_______________;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式_________________。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②的单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如下图所示,该物质的化学式为_________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com