
科目: 来源: 题型:
①若做化学实验时手指不慎被划破,可从急救箱中取FeCl3溶液应急止血 ②用氯化铁净水 ③在水泥厂、冶金工厂常用高压电对气溶胶作用除去大量烟尘 ④制肥皂时在高级脂肪酸钠、甘油和水形成的混合物中加入食盐析出肥皂 ⑤动植物尸体在土壤里的腐败 ⑥喝了含MgCl2的卤水,可以用牛奶或豆浆解毒
A.只有②③④ B.只有④⑤⑥
C.只有①②⑤ D.全部都是
查看答案和解析>>
科目: 来源: 题型:
A.二甘醇和丙二醇都是易溶于水的物质
B.丙二醇和丙三醇互为同系物
C.二甘醇和丙二醇都能和乙酸发生酯化反应
D.二甘醇和丙二醇都能发生催化氧化反应,最终生成二元羧酸
查看答案和解析>>
科目: 来源: 题型:
①取440 mL甲溶液与120 mL乙溶液反应,产生1.56 g沉淀;
②取120 mL甲溶液与440 mL乙溶液反应,产生1.56 g沉淀;
③ 取120 mL甲溶液与400 mL乙溶液反应,产生3.12 g沉淀。
通过必要的计算和推理判定:
(1)甲溶液为____________溶液,其物质的量浓度为____________mol·L-1。乙溶液为____________溶液,其物质的量浓度为____________mol·L-1。
(2)写出实验③的有关离子方程式:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(1)以丁烷代表汽油,这个电池放电时发生反应的化学方程式是:______________________。
(2)这个电池的正极发生的反应是:____________________,负极发生的反应是____________________;固体电解质里的O2-的移动方向是____________;向外电路释放电子的电极是____________________。
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是________________________________。
(4)你认为在ZrO2晶体里掺杂Y2O3,用Y3+代替晶体里的部分Zr4+对提高固体电解质的导电能力会起什么作用?其可能的原因是什么?_______________________________。
(5)汽油燃料电池最大的障碍是氧化反应不完全产生____________,堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,这正是新一代化学家的历史使命。
查看答案和解析>>
科目: 来源: 题型:
(1)若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应为____________________热反应。
(2)欲使起始反应维持向逆反应方向移动,则x的取值范围为___________________。
(3)在一定温度的上述平衡体系中,另按1∶2的物质的量比充入D、E两种气体(此时容器中气体的总量不要求保持12 mol)按下式发生反应:D(g)+E(g)![]() 2F(g),当反应达平衡时,D在这三种物质中的物质的量分数为p%。若向容器中投入m mol D、n mol F和一定量的E,在这三种物质的新平衡体系中D的物质的量分数为p%,则所投入E的物质的量为____________(今假设A、B、C与D、E、F间不发生的反应)。
2F(g),当反应达平衡时,D在这三种物质中的物质的量分数为p%。若向容器中投入m mol D、n mol F和一定量的E,在这三种物质的新平衡体系中D的物质的量分数为p%,则所投入E的物质的量为____________(今假设A、B、C与D、E、F间不发生的反应)。
查看答案和解析>>
科目: 来源: 题型:
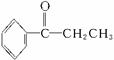
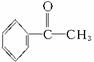
(1)现欲合成化合物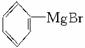 ,用格林试剂与相应的醛或酮加成,一共有?____________?种方法,试写出所用格林试剂与相应醛或酮的结构简式。
,用格林试剂与相应的醛或酮加成,一共有?____________?种方法,试写出所用格林试剂与相应醛或酮的结构简式。
_____________________________________________________________________
(2)试以苯、溴、乙烯、镁、水、空气等为主要原料,辅以必要的催化剂,合成化合物?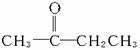 ,写出有关反应的化学方程式并注明反应条件。
,写出有关反应的化学方程式并注明反应条件。
___________________________,__________________________,________________________, ____________________,____________________。
查看答案和解析>>
科目: 来源: 题型:
(1)固体A属于________晶体,它的电子式为____________。
(2)A溶于水后,溶液呈___________性(填“酸”“碱”或“中”),其原因是_________________________________(用化学方程式表示)。
(3)A与铜或铜的某些化合物在一定条件下可合成CuH。CuH是一种难溶物,它能与盐酸
反应,放出气体,请写出这个反应的化学方程式:
______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:

它们在一定条件下有如下转化关系(反应中生成的水已略去):
(1)丙的名称是____________;C的化学式是____________;X属____________晶体。
(2)A+D→C的反应属于下列何种反应类型(填序号)____________。
A.化合反应 B.氧化还原反应
C.非氧化还原反应 D.离子反应
(3)工业生产中,将D转化为E的反应条件是____________________。
(4)写出A与H2O反应的化学方程式:______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
实验装置如下图:

实验步骤如下:
在实验装置的隔板上铺一层铜粒,打开A、B阀门,通入氧气,排除空气。关闭A、B阀,撤去氧气源。在漏斗中加入预先量好的硝酸,体积等于V(见上图),刚够淹没铜粒。先打开B阀,再打开A阀,让硝酸顺着漏斗颈流入试管,当硝酸与铜粒接触时马上关闭A阀。细心观察漏斗颈(以下称内管)中液面高低和试管(以下称外管)中溶液颜色及液面上方气体颜色的变化。
(1)描述观察到的实验现象
①_______________________________________________________________。
②_______________________________________________________________。
③_______________________________________________________________。
(2)写出实验过程中发生反应的化学方程式
①_______________________________________________________________。
②_______________________________________________________________。
③_______________________________________________________________。
(3)如果测得反应开始时液封内的气体体积是V1,反应结束后液封内的气体体积是V2(气体体积均已换算成标准状况),则反应后生成硝酸铜的物质的量是____________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com