
科目: 来源: 题型:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 255 | 385 | 459 |
气体体积/mL | 280 | 336 | 336 |
试完成下列问题:
(1)甲组实验中,盐酸(选填“过量”“适量”或“不足量”,下同)__________;乙组实验中盐酸____________。
(2)盐酸的物质的量浓度是多少?
(3)合金中镁、铝的物质的量之比为多少?
(4)丙实验之后,向容器中加入一定量的1.00 mol·L-1NaOH溶液,能使合金中的铝粉恰好完全溶解,再过滤出不溶性固体,求所得滤液中各溶质的物质的量浓度。
查看答案和解析>>
科目: 来源: 题型:
(1)当A、B、C三种单质放出的H2一样多时,____________________________________。
(2)当C单质与盐酸反应放出的H2最多时,_______________________________________。
(3)当A单质与盐酸反应放出的H2最多时,_______________________________________。
(4)当B、C两种单质分别与盐酸反应产生的H2几乎一样多时,______________________。
查看答案和解析>>
科目: 来源: 题型:
合成路线:

上述流程中:(Ⅰ)反应A→B仅发生中和反应,(Ⅱ)F与浓溴水混合不产生白色沉淀。
(1)指出反应类型:反应②_______________,反应④_______________。
(2)写出结构简式:Y_______________,F____________________________________。
(3)写出B+E→J的化学方程式_______________________________________________。
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式_____________、_______________、_______________。
查看答案和解析>>
科目: 来源: 题型:
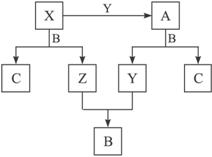
据此推断并完成下列各题:
(1)在A、B、C这三种化合物中,必定含有的元素是____________(用字母X、Y、Z来表示)。
(2)单质X必定是____________(填“金属”或“非金属”)。
(3)写出单质X和化合物B反应生成单质Z和化合物C的离子方程式(用具体物质的化学式表示):____________________________________________________________________。
(4)化合物A的化学式中,元素X和元素Y的原子个数比为_________。
查看答案和解析>>
科目: 来源: 题型:
(1)使温度和压强在上述条件下恒定不变,再往上述密闭容器内充入4 mol Z,则反应达到平衡时,容器的容积为___________________,Z的体积分数为___________________。
(2)若另选一容积固定不变的密闭容器,仍控制温度为T ℃,使4 mol X和2 mol Y反应达到平衡状态时,Z的体积分数仍为0.4,则该密闭容器的容积为___________________。
(3)若控制温度仍为T ℃,另选一容积为V L的固定不变的密闭容器,往其中充入一定量的X和Y,使反应达到平衡,这时Z的体积分数仍为0.4。则充入的X和Y的物质的量应满足的关系是:an(Y)<n(X)<bn(Y),其中a为___________________,b为___________________。
查看答案和解析>>
科目: 来源: 题型:
(1)电解时的电极反应:阳极__________________,阴极_____________________。
(2)![]() 转变成Cr3+的离子反应方程式:_______________________________________。
转变成Cr3+的离子反应方程式:_______________________________________。
(3)电解过程Cr(OH)3、Fe(OH)3沉淀是怎么产生的?________________________________
_____________________________________________________________________。
(4)能否用Cu电极来代替Fe电极?_______,(填“能”或“不能”),简述理由____________
_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)加入KI溶液,血红色褪去;
(2)加入少量酸性的高锰酸钾溶液,血红色褪去;
(3)加入氰化钾固体,溶液的血红色褪去;若先在足量的盐酸溶液中加入氟化钾固体,再与上述血红色溶液混合,溶液的血红色不消失。
问题:思考产生上述现象的原因是什么?如何对(1)设计实验证明你的观点?
查看答案和解析>>
科目: 来源: 题型:
下图为某实验者设计的验证银圆完全溶解于一定量的浓硝酸,生成的NO2气体中含有NO的实验装置图。
常温时,NO2与N2O4混合存在;在低于0 ℃时,几乎只有无色N2O4晶体存在。
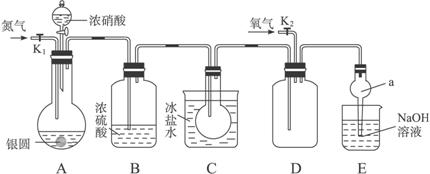
(1)反应前先打开A部分的活塞K1,持续通一段时间N2,其理由是_______________________
_____________________________________________________________________。
(2)若装置中缺B部分,其后果是_________________________________________________。
(3)反应结束后,打开D部分的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是_____________________________
_____________________________________________________________________。
(4)E部分中a仪器所起的作用是_________________________________________________。
(5)已知该银圆的质量为25 g,加入75 mL 12 mol·L-1的浓硝酸。实验结束后,A部分烧瓶内溶液中H+的浓度为2 mol·L-1(反应中HNO3既无挥发也无分解),体积仍为75 mL。
①参加反应的硝酸的物质的量为_________________________。
②为测定该银圆中铜的质量分数,还须进行的主要实验操作是_________________________。
查看答案和解析>>
科目: 来源: 题型:
A.HCOOCH3 B.CH3CHO C.HOOCCOOH D.C6H12O6
查看答案和解析>>
科目: 来源: 题型:
(1)将镁粉投入冷水中,未见明显现象;(2)将镁粉投入FeCl3溶液中,观察到有气泡产生,溶液颜色逐渐变浅,同时逐渐产生红褐色沉淀。则下列有关镁与FeCl3溶液反应的叙述中正确的是
A.镁只与FeCl3溶液中的Fe3+直接反应
B.气泡是镁与FeCl3溶液中的水直接反应产生的
C.红褐色沉淀是镁与水反应生成的Mg(OH)2与Fe3+反应所得
D.气泡是镁与FeCl3水解生成的盐酸反应产生的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com