
科目: 来源: 题型:
A.分解H2O2制O2,每生成1 mol O2转移4NA个电子
B.25 ℃时1 L pH=7的醋酸与醋酸钠的混合溶液中,一定有10-7NA个醋酸分子被电离
C.标准状况下,22 g C3H8与N2O混合气体所占体积约为11.2 L
D.用惰性电极电解1 L浓度均为2 mol·L-1的AgNO3与Cu(NO3)2混合溶液,当有0.2NA个电子发生转移时,阴极析出6.4 g金属
查看答案和解析>>
科目: 来源: 题型:
A.羊毛与聚酯纤维的化学成分相同 B.聚酯纤维和羊毛在一定条件下均能水解
C.纯羊毛为纯净物 D.羊毛与聚酯纤维不能用燃烧法区别
查看答案和解析>>
科目: 来源: 题型:
A.13C与12C的化学性质不同 B.15N的核外电子数与中子数相同
C.13C与15N的中子数相同 D.13C与12C互为同位素
查看答案和解析>>
科目: 来源: 题型:
A.全氟辛酸铵(C7F15COONH4)的制取反应:
C7F15COOH+NH3·H2O![]() C7F15COONH4+H2O
C7F15COONH4+H2O
B.全氟辛酸铵(C7F15COONH4)在加热的条件下不会发生分解
C.氟的聚合物具有耐高温性、抗导电性和低燃性
D.经常以铁锅烹饪食物,有助于防治缺铁性贫血
查看答案和解析>>
科目: 来源: 题型:
![]()
其中反应②为:4NO+3O2+2H2O====4HNO3,原料气为氨气和空气的混合物,假设空气中氧气的体积分数为0.2。
(1)写出反应①的化学方程式____________________________________________________。
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中制备硝酸的氨气(不包含第③步被硝酸吸收的氨气)的体积分数最大值为__________。
(3)若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为多少?在合成硝酸铵的全流程中,氨气的总利用率为多少?(请写出该小题的计算过程)
查看答案和解析>>
科目: 来源: 题型:
(1)若固体恰好完全溶解,消耗硫酸的体积为0.3 L,且所得溶液中无Fe3+,则a=__________,混合粉末中铜的质量为___________。
(2)若将固体完全溶解于1.00 L上述硫酸中,测得c(Fe3+)=0.1 mol·L-1(假设反应前后溶液的体积不变),则混合粉末中铜的质量的最大值为_________g。
(3)若固体恰好完全溶解,消耗硫酸的体积为0.3 L,且所得溶液中既有Fe3+,也有Fe2+,则a的取值范围是_________。
查看答案和解析>>
科目: 来源: 题型:

已知(1) 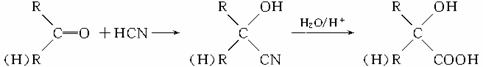
(2)CH3COOCH2CH2OH的名称为乙酸羟乙酯。
试完成:
(1)A、E的结构简式分别为:A________________________,E________________________。
(2)写出下列反应的反应类型:C→D____________________,E→F___________________。
(3)写出下列转化的化学方程式:
I→G______________________________________________;
G+F→H________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
![]()
某有机物的结构简式为: ,当它与等物质的量的Br2的水溶液发生加成反应时有5种产物,请补写其他3种产物的结构简式。
,当它与等物质的量的Br2的水溶液发生加成反应时有5种产物,请补写其他3种产物的结构简式。

查看答案和解析>>
科目: 来源: 题型:
①混合溶液中水电离出的c(H+)______________0.2 mol·L-1HCl溶液中水电离出的c(H+);(填“>”“<”或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)—c(M+)=_______________mol·L-1 c(H+)—c(MOH)=_______________mol·L-1
(2)室温下如果取0.2 mol·L-1MOH溶液与0.1 mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度__________MCl的水解程度(填“>”“<”或“=”),溶液中各离子浓度由大到小的顺序为______________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)C元素在周期表中的位置是___________________;C在A中燃烧形成的固体中阴阳离子的数目比为_____________;液态X类似B2A,也能微弱电离且产生电子数相同的两种离子,则液态X电离方程式为_____________________________________________________。
(2)M、N是由A、B、C、D四种元素中任意三种元素组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且物质的量浓度相等的M、N溶液中水的电离程度,前者小于后者。则M、N分别为_______(填化学式);若将0.1 mol·L-1M和0.2 mol·L-1N两溶液等体积混合,所得溶液中离子浓度的大小顺序为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com