
科目: 来源: 题型:
A.往氢硫酸溶液中加入稀盐酸,c(S2-)降低?
B.温度不变时,敞口久置于空气中的饱和硝酸钾溶液中会有晶体析出?
C.在合成氨的工业生产中,使用较高的温度,有利于提高产量??
D.在密闭容器中,水面上的蒸气压随温度升高而增大?
查看答案和解析>>
科目: 来源: 题型:
A.低温、高压、适当的催化剂?
B.高温、常压?
C.尽可能高温、高压?
D.适当的温度、适当的高压、适宜催化剂?
查看答案和解析>>
科目: 来源: 题型:
A.加入催化剂有利于合成氨的反应?
B.高压有利于合成氨的反应?
C
D.将混合气体中的氨气液化有利于合成氨反应
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
![]()
已知常压下SO3体积分数为91%,试回答:?
(1)在生产中常用过量的空气是为了 。?
(2)加热到400~
(3)压强应采用(填“高压”或“常压”) ,原因是? 。?
(4)常用浓H2SO4来吸收SO3,而不是用水,是因为 。?
(5)尾气中的SO2必须回收,是因为 。?
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0?
2SO3(g);ΔH<0?
(1)降低温度,二氧化硫转化率 ,化学反应速率 。(以上均填“增大”“减小”或“不变”)
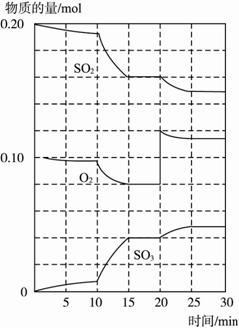
图9-13
(2)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图9-13,反应处于平衡状态的时间是 。?
(3)据图判断,反应进行至20 min时,曲线发生变化的原因是________________________(用文字表达),10 min到15 min的曲线变化的原因可能是(填写编号)。?
a.加了催化剂
b.缩小容器体积?
c.降低温度
d.增加SO3的物质的量
查看答案和解析>>
科目: 来源: 题型:
(2)若a=0.5,b= 和c= 。?
(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c): 。??
查看答案和解析>>
科目: 来源: 题型:
(1)SO2的平衡浓度为0.05 mol·L-1??
(2)O2的转化率α(O2)=40%?
(3)平衡时混合气的总量为3.4 mol。?
(4)SO3在平衡混合气中的含量为50%。?
(5)平衡混合气的平均相对分子质量为60。?
(6)O2的平衡浓度为0.11 mol·L-1??
(7)达平衡时容器内压强减小了1/5。?
(8)若保持容器压强不变,则达平衡时容器体积变为9 L。???????????
查看答案和解析>>
科目: 来源: 题型:
编号 | 起始状态时物质的量/mol | 平衡时HBr 物质的量/mol | ||
H2 | Br2 | HBr | ||
已知 | 1 | 2 | 0 | a |
(1) | 0.5 | 1 | 0 |
|
(2) |
|
| 1 | |
(3) | n | m(m≥2n) |
|
|
在(3)的推算过程中,设起始状态时HBr物质的量为x,平衡时HBr物质的量为y,请写出求x、y依据的两个比例式。????????
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com