
科目: 来源: 题型:
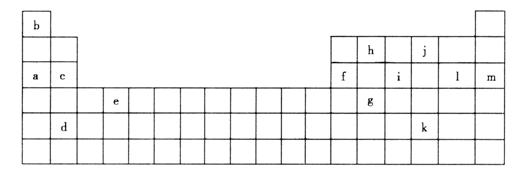
(1)下列__________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外`
电子离开该原子或离子所需要的能量主要受两大因素的影响:
a.原子核对核外电子的吸引力 b.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1)
| 锂 | X | Y |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7296 | 4570 | 1820 |
失去第三个电子 | 11799 | 6920 | 2750 |
失去第四个电子 |
| 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量远远大于失去第一个电子所需的量____________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成化合物的化学式____________________。
③Y是周期表中__________族元素。
④以上13种元素中__________(填字母)元素原子失去核外第一个电子需要的量最多。
查看答案和解析>>
科目: 来源: 题型:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是__________(填氧化剂或还原剂)。
(2)写出CuH在氯气中燃烧的化学反应方程式____________________。
(3)CuH溶解在稀盐酸中生成的气体是__________(填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中只生成NO气体,请写出CuH溶解在足量稀硝酸中反应的化学方程式_____________________________。
查看答案和解析>>
科目: 来源: 题型:
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
M(混合物) | 9.2g | 15.7g | 27.6g |
VCO2(标况) | 2.24L | 3.36L | 3.36L |
A.盐酸的物质的量浓度为3.0 mol/L
B.能计算出混合物中NaHCO3的百分含量
C.加入混合物9.2 g时盐酸未反应完
D.15.7 g混合物恰好与盐酸完全反应
查看答案和解析>>
科目: 来源: 题型:
A.NaHCO3 B.Na2CO3 C.Ca(OH)2 D.NaCl
查看答案和解析>>
科目: 来源: 题型:
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
A.112 B.73 C.64 D.65
查看答案和解析>>
科目: 来源: 题型:
A.14:13:12:1 B.1:12:13:14
C.1:10:100:1 000 D.1 000:100:10:1
查看答案和解析>>
科目: 来源: 题型:
A.负极反应为14H2O+7O2+28e-====28OH-
B.放电一段时间后,负极周围的pH升高
C.放电过程中KOH的物质的量浓度不变
D.每消耗1 mol C2H6,则电路上转移的电子为14 mol
查看答案和解析>>
科目: 来源: 题型:
A.标准状况下,参加反应的CO2体积为0.224 AL
B.用上述数据不能确定NaOH溶液的物质的量浓度
C.若A=B,则CO2与NaOH溶液反应的产物只有Na2CO3
D.B不可能大于A
查看答案和解析>>
科目: 来源: 题型:
A.0.4 mol B.0.6 mol C.0.8 mol D.1.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com