
科目: 来源: 题型:
实验序号 | 样品质量/g | Ba(OH)2溶液的体积/L | 沉淀质量/g |
1 | 0.858 | 0.5 | 1.379 |
2 | 1.716 | 0.5 |
|
3 | 2.574 | 0.5 | 4.137 |
4 | 3.432 | 0.5 | 5.516 |
5 | 4.290 | 0.5 | 5.516 |
回答下列问题:
(1)第2次实验中产生沉淀________g。
(2)样品中NaHCO3和K2CO3的物质的量之比是________。
(3)室温下取第3组实验所得溶液体积的![]() ,加水配成500mL溶液,则稀释后溶液的pH为________。
,加水配成500mL溶液,则稀释后溶液的pH为________。
查看答案和解析>>
科目: 来源: 题型:
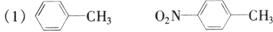
利用这些反应,按下图所示步骤可以从烃A合成一种外科用药的中间体X。(下列步骤中未标出的试剂和反应条件已略去)
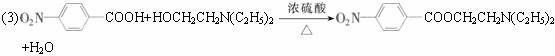
请回答下列问题:。
(1)写出下列物质的结构简式:A.______________,B.________________D________________。
(2)反应①—④中属于取代反应的是(填反应代号)________________,反应⑤的类型为________________。
(3)写出C+E![]() F的化学方程式__________________________。
F的化学方程式__________________________。
查看答案和解析>>
科目: 来源: 题型:
完成下列有关问题:
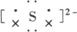
(1)X的电子式为________,G的晶体类型为________。
(2)反应①的反应条件是________________________________。
(3)写出反应②的化学方程式:____________________________________________________。
(4)写出反应③的离子方程式:____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)相同温度下,在乙中加入4 mol N2、6 mol H2,若乙的压强始终与甲的压强相等,乙中反应达平衡时,生成NH3的物质的量为________mol(从下列各项中选择,只填序号,下同);若乙的容积与甲的容积始终相等,乙中反应达平衡时,生成NH3的物质的量为________mol。
A.小于m B.等于m C.在m—2m之间
D.等于2m E.大于2m
(2)相同温度下,保持乙的容积为甲的一半,并加入1 mol NH3,要使乙中反应达平衡时,各物质的体积分数与上述甲容器中达平衡时相同,则起始应加入______molN2和______mol H2。
查看答案和解析>>
科目: 来源: 题型:

①配制0.1 mol·L-1盐酸和0.1 mol·L-1 NaOH溶液;
②取一片此胃药片(药片质量均相等,每片为0.2g),磨碎后转移至锥形瓶中;
③以酚酞为指示剂,用0.1 mol·L-1 NaOH溶液滴定,用去Vx mL NaOH溶液时达到滴定终点;
④加入25 mL 0.1 mol·L-l盐酸。
(1)为使测定结果准确,至少需要滴定两次,得到的Vx值分别为Vl和V2。写出全部实验过程中,各步操作的正确顺序(填编号):_________。
(2)图中所示仪器中,配制0.1 mol·L-1盐酸和0.1 mol·L-1 NaOH溶液肯定不需要的仪器是是________(填序号);配制上述溶液还需要用到的玻璃仪器是________(量取液体的仪器除外)________________(填仪器名称)。
(3)写出相关化学方程式:_________________________________________________________
____________________________________________________________________。
(4)每片胃药中含CaCO3的质量为________________g。
查看答案和解析>>
科目: 来源: 题型:
A.只将无水乙醇与冰醋酸混合制取乙酸乙酯
B.用蒸馏水鉴别甲醇、乙醛、溴苯三种液体
C.用碱式滴定管量取12.50mL 0.2mol·L-1的KMnO4溶液
D.用分液漏斗分离硝基苯和水
E.苯酚不慎沾在手上,马上用NaOH溶液冲洗
F.用铁粉和浓溴水、苯放入烧瓶中反应制取溴苯
G.制备氢氧化铁胶体时,应往沸水中滴加FeCl3饱和溶液,并继续加热到溶液呈红褐色为止
查看答案和解析>>
科目: 来源: 题型:
A.金属锂作电池的正极,石墨作电池的负极
B.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
C.电解质溶液中混入水,对电池反应无影响
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1
查看答案和解析>>
科目: 来源: 题型:
A.(b-2a)mol B.![]() bmol C.
bmol C.![]() ·a mol D.2a mol
·a mol D.2a mol
查看答案和解析>>
科目: 来源: 题型:
A.25℃时,饱和KCI溶液的浓度大于4.0 mol·L-1
B.此溶液中KCI的质量分数为了![]()
C.20℃时,密度小于1.174 g·cm-3的KCI溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
查看答案和解析>>
科目: 来源: 题型:
A.c=a+b B.c=2b-a C.c=a+2b D.c=2a-b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com