
科目: 来源: 题型:
A.Y的单质是原子晶体
B.X的单质固态时为分子晶体
C.X与碳形成的化合物为分子晶体
D.X与Y形成的化合物固态时为分子晶体
查看答案和解析>>
科目: 来源: 题型:
A.CaO B.浓硫酸 C.NaCl D.碱石灰
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
请回答:(1)根据上述两种不同操作过程及实验数据可判断甲溶液是___________,乙溶液是___________。
(2)用离子方程式表示两次操作得到不同气体体积的原因:
①_______________________________________________;
②_______________________________________________。
(3)甲溶液的物质的量浓度为___________mol·L-1,乙溶液的物质的量浓度为_______mol·L-1(CO2在水溶液中的少量溶解忽略不计)。
(4)将n mL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体;积为V mL(标准状况),则y的取值范围为___________。
查看答案和解析>>
科目: 来源: 题型:
已知A是CH2=CH2,F是![]() 且醛或酮具有如下性质:
且醛或酮具有如下性质:
 化合物B仅含碳氢氯三种元素,其式量接近65。
化合物B仅含碳氢氯三种元素,其式量接近65。
下列是由乙烯制备乳酸的三种不同途径。
A![]() B
B![]() C
C![]()
![]() E
E![]()
![]()
![]()
(1)乳酸不可能发生的反应是___________(填序号)。
①取代反应 ②酯化反应 ③水解反应 ④消去反应 ⑤聚合反应 ⑥中和反应
(2)乳酸自身在不同条件下可形成不同的酯,请分别写出三种结构类型不同的酯的结构简式:______________________,______________________,______________________。
(3)写出下列转化的化学方程式
①A![]() C____________________________________________。
C____________________________________________。
②A![]() D____________________________________________。
D____________________________________________。
③D![]() E____________________________________________。
E____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)加入3 mol SO2和2 mol O2发生反应,达到平衡时,放出的热量为___________。
(2)保持温度不变,在相同的容器中,将起始物质物质的量改为a mol SO2、b mol O2、c mol SO3(g)(c>0),欲使平衡时SO3的体积分数为![]() ,O2的体积分数为
,O2的体积分数为![]() ,则:
,则:
①达到平衡时,(1)与(2)放出的热量___________(填序号)。
A.相等 B.前者小于后者
C.前者大于后者 D.无法确定
②a、b、c必须满足的关系是(一个用a、c表示,另一个用b、c表示)___________,__________。
查看答案和解析>>
科目: 来源: 题型:
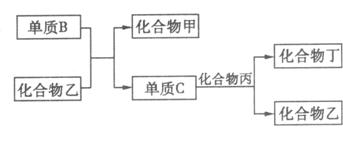
(1)根据以上条件,可以确定A、B、C、D四种元素中三种,不能被确定的第四种元
素是___________,写出转化关系图中已确认的反应的化学方程式:____________________。
(2)下列四个补充条件中的任何一个都可以进一步确定第四种元素,但其中一个条件推断的第四种元素与其余三个条件推断出的第四种元素不同,则此条件是________________________。
A.化合物甲与丙、乙与丙均能够发生反应
B.化合物甲、乙、丙都是无色物质,其中只有甲有刺激性气味
C.通常情况下乙和丁不发生反应,若将乙、了、单质C混合,立即发生反应
D.单质C和化合物丁不能共存
依据该条件推断,第四种元素在周期表中的位置为___________。
(3)由(2)中的另外三个补充条件推断出的第四种元素所形成化合物丙的空间构型为______________________。
查看答案和解析>>
科目: 来源: 题型:

回答下列问题:
(1)实验开始时,欲使装置中的稀硫酸和黄铜中的锌发生反应,应进行的操作是____________
______________________;反应结束后,恢复至反应前的温度,对碱式滴定管进行准确读数前,应进行的必要操作是:______________________________________________________
(2)为了保证实验结果的准确,请你将本实验过程中需直接测定的有关物理量填入下表中(用文字说明,不必填满):
① | ② | ③ | ④ | ⑤ | ⑥ |
|
|
|
|
|
|
(3)某同学还想利用托盘天平和下图所示装置完成锌的质量分数和锌的相对原子质量的测定实验。

①该实验过程中,必须对反应后所剩的固体进行洗涤、干燥,如何确定所得固体是干燥的_____________________________________________________________________。
②请你从该实验装置、中学化学实验室的现有条件两方面,对该实验方案的可行性进行评价:___________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)除去AgI胶体中混有的I-离子___________。
(2)除去苯中含有的少量苯酚____________________
(3)分离CuSO4·5H2O和BaSO4的混合物___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com