
科目: 来源: 题型:
A.它一定含有3个中子 B.它比一个普通氢分子多一个原子核
C.它的构成可以用![]() 表示 D.可以推测它的化学性质与H2不同
表示 D.可以推测它的化学性质与H2不同
查看答案和解析>>
科目: 来源: 题型:
A.水的密度比柴油的大 B.水不能燃烧
C.催化剂可以改变反应速率 D.催化剂不能使本来不存在的反应发生
查看答案和解析>>
科目: 来源: 题型:
A.同系物 B.同分异构体
C.同位素 D.同素异形体
查看答案和解析>>
科目: 来源: 题型:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20gA全部溶于0.15 L 6.0 mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标准状态)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填写:
(1)产物中的单质B是___________________________;
(2)③中所发生的各反应的离子方程式是____________________________________;
(3)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为__________________,c(Fe2+)为__________________。
查看答案和解析>>
科目: 来源: 题型:

(1)G的化学式为___________________________;
(2)Z的电子式为___________________________;
(3)写出下列反应的化学方程式:
反应①:_________________________________________________________;
反应④:_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A(g)+B(g)![]() C(g)
C(g)
(1)若开始时放入1 mol A和1 mol B,到达平衡后,生成a molC,这时A的物质的量为_________mol。
(2)若开始时放入3 mol A和3 mol B,到达平衡后,生成C的物质的量为__________mol。
(3)若开始时放入x molA、2molB和1 molC,到达平衡后,A和C的物质的量分别为y mol和3a mol,则y=_________mol。
平衡时,B的物质的量_________(选填一个编号)。
甲大于2mol 乙小于2mol
丙等于2mo1 丁可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3 molC,待再次到达平衡后,C的物质的量分数是_________。
查看答案和解析>>
科目: 来源: 题型:
(1)发射“神六”的高能燃料是偏二甲肼(分子式为C2H8N2)。已知偏二甲肼分子中有一个氮原子不与氢原子相连,其分子结构简式为___________________________。
又知1mol液态偏二甲肼与足量液态的N2O4完全反应放出Q kJ热量,产物为二氧化碳、氮气和水蒸气。试写出该反应的热化学方程式____________________________________。
(2)“神六”表面覆盖了景德镇制造的可耐2000℃高温的氮化硅陶瓷,已知氮化硅晶体结构中,原子间都以单键相连且N、N间和Si、Si间不直接相连,同时每个原子都满足8个电子的稳定结构。则氮化硅的化学式为__________________,氮化硅晶体应属于_________晶体。
(3)“神六”进入轨道后,主要是利用太阳能和氢氧燃料电池并通过九江制造的导电滑环来为整个飞船提供能源。已知氢氧燃料电池的负极反应式为:H2-2e-+2OH-====2H2O则正极的反应式为:___________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)高碘酸是_________(填“强酸”或“弱酸”),理由是___________________________。
(2)0.01 mol/L的碘酸(HIO3)溶液与pH=12的NaOH的溶液等体积混合所得溶液中![]() 与Na+的浓度关系是_________(填“大于”“小于”或“等于”)。
与Na+的浓度关系是_________(填“大于”“小于”或“等于”)。
(3)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,该反应的离子方程式可表示为____________________________________。
查看答案和解析>>
科目: 来源: 题型:
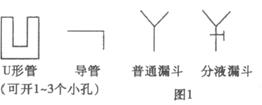
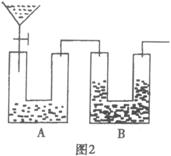
某同学用图2测定Na2CO3试样的纯度(杂质不与水反应),其中A容器中盛有Na2CO3样品10.0g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。他利用碱石灰的增重求出纯净的Na2CO3质量,再求纯度。他重复正确操作了三次,结果数据出现了较大偏差(设原容器中CO2气体的含量可忽略不计,各容器内反应完全,下同)
(1)请你分析出现较大偏差的原因__________________________________________________。
通过仔细分析,该同学重新设计了一套实验装置(见图3)。(实验室中可供选择的试剂和药品还有Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水)

(2)该同学新设计的装置仍不完整,应在_________处(填B或D)添加_________(写出装置及药品的名称)。
(3)A装置中分液漏斗所盛液体为_________,F装置在整套装置中的作用是_______________
_____________________________________________________________________。
(4)如果B、D内不设计任何装置而直接连通A、C、E,则实验结果将_________(填偏高、偏低、无影响)。
查看答案和解析>>
科目: 来源: 题型:
a量筒 b容量瓶 c滴定管 d托盘天平 e温度计
(1)其中标示出仪器使用温度的是_________(填写编号)。
(2)由于操作错误,使得到的数据比正确数据偏小的是_________(填写编号)。
A.实验室制乙烯测量混合液温度时,温度计的水银球与烧瓶底部接触
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容所得溶液的浓度
(3)称取10.5 g固体样品(1 g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com