
科目: 来源: 题型:
A.0.1 mol F-中含有的电子数为9 NA
B.1 L0.5 mol/L的CaCl2溶液中含有的Cl-数为0.5NA
C.常温常压下,32 gO2中所含的质子数为16NA
D.标准状况下,11.2L的CH4中含有的氢原子数为NA
查看答案和解析>>
科目: 来源: 题型:
A.从尿液中分离出的“青春素”是一种对人体有益的元素
B.长期饮用纯净的蒸馏水比饮用矿泉水对人体有益
C.负氧离子发生器只产生O3,对人体有益无害
D.某地区冬季空气中可悬浮颗粒的含量比夏季高,主要原因是冬季煤的使用量增大
查看答案和解析>>
科目: 来源: 题型:
Cu2O+Fe2(SO4)3+H2SO4![]() CuSO4+FeSO4+H2O。反应生成的硫酸亚铁用硫酸酸化了的高锰酸钾溶液进行滴定,其滴定反应的化学方程式为(未配平):
CuSO4+FeSO4+H2O。反应生成的硫酸亚铁用硫酸酸化了的高锰酸钾溶液进行滴定,其滴定反应的化学方程式为(未配平):
KMnO4+H2SO4+FeSO4![]() Fe2(SO4)3+MnSO4+K2SO4+H2O
Fe2(SO4)3+MnSO4+K2SO4+H2O
若每升滴定剂溶液中含有0.400 mol KMnO4,求该KMnO4溶液对Cu2O的滴定度。
查看答案和解析>>
科目: 来源: 题型:阅读理解
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。2005年的《化学教育》报道了如下实验研究:
实验一、定性研究:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
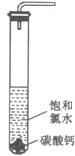
请回答:
(1)反应后所得的溶液漂白性增强的原因是__________________________________________;
(2)依据上述实验可推知,②的滤液中的溶质除CaCl2、HClO外,还含有________________。
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150 mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加。
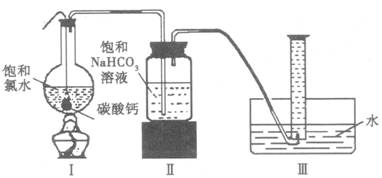
请回答:
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是___________________________________;
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少A g,总共收集到标准状况下的CO2气体B L,发现![]() 明显小于
明显小于![]() 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是_______________
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是_______________
_____________________________________________________________________;(5)实验后发现,装置Ⅱ中的液体增多了,其原因是__________________________________
____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)若平衡时,甲、乙两容器中A的物质的量相等,则x=____________;若平衡时,甲、乙两容器中A的物质的量不相等,则x=______________。
(2)平衡时甲、乙两容器中A、B的物质的量之比是否(填“是”或“否”)_______相等。平衡时甲中A的体积分数为__________。
(3)若平衡时两容器中的压强不相等,则两容器中压强之比为__________。
查看答案和解析>>
科目: 来源: 题型:
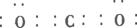
(1)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行。E的水溶液显酸性,其原因是(用离子方程式表示)______________;已知1 gD与F反应生成B时放出92.3 kJ热量,写出该反应的热化学方程式_____________________________。
(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,原子核外最外层电子数D是A的2倍,③④反应中都有红棕色气体生成,②③④反应中的部分产物已略去。A中元素在元素周期表中的位置是______________;D的电子式是__________;在②③④反应中F既表现氧化性又表现酸性的是(填序号) ______________。
查看答案和解析>>
科目: 来源: 题型:
①A+B![]() M+D+E ②M+E
M+D+E ②M+E![]() A+F+B
A+F+B
请针对以下两种不同情况回答:
(1)A是一种钠盐,反应①是化学工业上制取单质E和化合物M的重要方法。A的化学式为______________,反应②的离子方程式为______________。
(2)当A是一种铜盐时,A中的酸根离子可以是下列的_______(填序号);
①Cl- ②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
若该铜盐中的一个酸根离子共含有50个电子,则反应②的化学方程式为________________
___________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
例如:RCH=CHR′![]() RCHO+R′CHO
RCHO+R′CHO
下列框图中方框内的字母各代表一种芳香族化合物,其中B的结构中不含甲基,D的分子式为C9H8O2。A转化为B时,A与H:的物质的量之比为1:2(下列物质间转化中有的需要加热)。

请回答下列问题:
(1)A的分子式为______________,F的结构简式为______________。
A![]() C的化学方程式为______________________________________。
C的化学方程式为______________________________________。
(2)B的某些同分异构体能跟浓溴水反应。其中1 mol某同分异构体跟浓溴水反应时,需消耗3 mol Br2,且该同分异构体分子中含有一个甲基,则其结构简式为
_______________________________________________________________。
(3)A是一种可以作为药物的有机物,将A在一定条件下氧化后可以得到两种有机酸X和Y,其中Y是二元酸。则X的结构简式为______________,Y的结构简式为______________。
查看答案和解析>>
科目: 来源: 题型:
A.HC≡CH+ROH![]() CH2=CHOR
CH2=CHOR
B.HC≡CH+HCHO![]() HC≡CCH2OH
HC≡CCH2OH
C.R2NCH2OH+HC≡CH![]() R2NCH2C≡CH+H2O
R2NCH2C≡CH+H2O
D.R2NH+HC≡CH![]() R2NCH=CH2
R2NCH=CH2
(1)以上反应中属于加成反应的有(填序号)______________。
(2)现有下列转化:

所得高聚物用途十分广泛,涉及到化妆品乳化剂、染料的分散剂、酒类的澄清剂等。写出下列物质的结构简式:E______________,F______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com