
科目: 来源: 题型:
A.溶液中c(H+)和c(OH-)都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
查看答案和解析>>
科目: 来源: 题型:
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++![]() ====BaSO4↓+H2O
====BaSO4↓+H2O
B.NH4HCO3溶液与过量NaOH溶液反应:![]() +OH-==== NH3↑+H2O
+OH-==== NH3↑+H2O
C.苯酚钠溶液中通入少量![]() +
+![]()
D.FeBr2溶液中通入少量Cl2:2Fe2++2Br-+2Cl2====2Fe3++Br2+4Cl-
查看答案和解析>>
科目: 来源: 题型:
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
查看答案和解析>>
科目: 来源: 题型:
(1)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为____________,其分子属于______________(填“极性”“非极性”)分子。
(2)E是非金属元素,但能表现出一些金属元素的性质,请写出单质E与氢氧化钠溶液反应的离子方程式_____________________________________________________________________。
(3)一定条件下,A的气体单质与B的气体单质充分反应生成6.
(4)A的单质与c的单质在KOH的浓溶液中可以形成原电池,如果以M和N为惰性电极,在电池的M极通入A气体,N极通入C气体,则N极的电极反应式为____________________。
(5)在
查看答案和解析>>
科目: 来源: 题型:
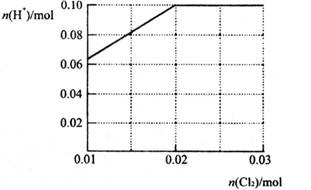
(1)按要求写出反应方程式:
①Cl2与H2SO3溶液反应的化学方程式_____________________________________________;
②Cl2与HBr反应的离子方程式___________________________________________________。
(2)请完成此过程溶液中n(H+)与Cl2用量n(Cl2)的关系曲线
(3)若反应后溶液的体积为1000 mL,则反应后溶液的pH为__________。
查看答案和解析>>
科目: 来源: 题型:
①1 mol A+2 mol NaOH→盐
②A+RCOOH(或ROH)![]() 有香味的物质 (R为烃基)
有香味的物质 (R为烃基)
![]()
④A的分子内脱水产物(不是环状化合物)可使溴水褪色
回答下列问题:
(1)A分子中含有官能团的名称为_________________________________________________。
(2)②,④反应的反应类型属于______________________,___________________反应。
(3)符合上述性质的A的同分异构体有(写结构简式)__________________________________。
(4)写出④反应即A分子内脱水产物与溴水反应的化学方程式(只写一个)________________。
查看答案和解析>>
科目: 来源: 题型:
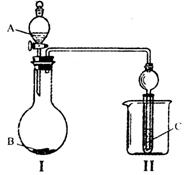
(1)若A为浓硫酸,B为金属铜(可对装置I加热),C为品红溶液。在实验中可观察到品红溶液褪色。则I中发生反应的化学方程式为_________。反应完全后往烧杯中加入沸水,可观察到试管中的现象为__________________。
(2)若A为盐酸,B为Na2CO3,C为苯酚钠溶液。
在实验中可观察到试管中的现象是__________________。然后往烧杯中加入沸水,又观察到试管中的现象是_________。要证明酸性强弱顺序:盐酸>碳酸>苯酚。该装置不够完整,还需进行的改进是_________。
(3)若B是生石灰,实验中可观察到:C溶液中先产生沉淀,然后沉淀溶解。当沉淀恰好完全溶解后,关闭分液漏斗活塞,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜。则A是__________________,C是______________和葡萄糖的混合液。该实验装置I中能产生气体的原因是_____________________。
(4)装置Ⅱ中球形漏斗的作用是_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,各物质相互转化关系如图所示。

回答下列问题:
(1)Z的化学式为_________________,G的化学式为__________________。
(2)H的电子式为_________________________________________________。
(3)写出X、B分别跟水反应的化学方程式:
X+H2O_________________________________________________________。
B+H2O_________________________________________________________。
(4)写出C+G→E的离子反应方程式:______________________________。
查看答案和解析>>
科目: 来源: 题型:
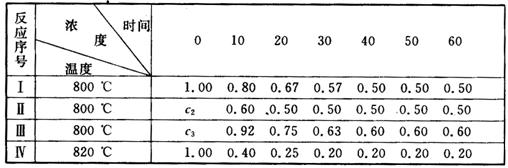
A.实验Ⅰ中20至30分钟内平均反应速率为vA=0.01 mol(L·min)
B.若实验Ⅱ中A的初始浓度c2为1.00 mol/L,则反应经20分钟达平衡且使用了催化剂
C.若实验Ⅱ中c2为1.00 mol/L,则实验Ⅲ中A的初始浓度c3肯定大于c2
D.由实验Ⅳ和实验I的数据比较,可推知该反应的正反应是放热反应
查看答案和解析>>
科目: 来源: 题型:
A.向氢氧化钠溶液中通入过量CO2:2OH-+CO2====![]() +H2O
+H2O
B.硫酸铝溶液中加入过量氨水:Al3++4 NH3·H2O====![]() +4
+4![]() +2H2O
+2H2O
C.用石墨作电极电解饱和食盐水:2Cl-+2H2O![]() 2 OH-+H2↑+Cl2↑
2 OH-+H2↑+Cl2↑
D.氢氧化亚铁溶于足量稀硝酸:Fe(OH)2+2H+====Fe2++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com