
科目: 来源: 题型:

图Ⅰ
图Ⅱ
(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是_______(选填“A”“B”或“C”)。
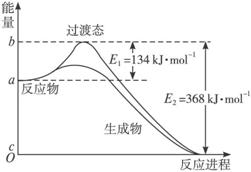
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。
图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________________________。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图Ⅱ中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/kJ·mol-1 | 197 | 360 | 499 | X |

图Ⅲ
已知白磷的燃烧热为2 378.0 kJ·mol-1,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中X=_________。
查看答案和解析>>
科目: 来源: 题型:
![]() Na2SO3+
Na2SO3+![]() KIO3+
KIO3+![]() ——
——![]() Na2SO4+
Na2SO4+![]() K2SO4+
K2SO4+![]() I2+
I2+![]() H2O
H2O
(1)配平上面的氧化还原反应方程式,将化学计量数填入方框中。
(2)其中氧化剂是_________,若反应中有5 mol电子转移,则生成的碘是________mol。
(3)该反应的过程和机理较复杂,一般认为发生以下①~④反应:
①![]() +
+![]()
![]()
![]() +
+![]() (反应速率慢)
(反应速率慢)
②![]() +
+![]()
![]() I-+2
I-+2![]() (反应速率快)
(反应速率快)
③5I-+6H++![]()
![]() 3I2+3H2O(反应速率快)
3I2+3H2O(反应速率快)
④I2+![]() +H2O
+H2O![]() 2I-+
2I-+![]() +2H+(反应速率快)
+2H+(反应速率快)
根据上述步骤推测该反应总的反应速率由反应________决定(填序号)。
(4)若预先加入淀粉溶液,由上述四步反应可以看出必须在________离子消耗完全时,才会有使淀粉变蓝的现象产生。
查看答案和解析>>
科目: 来源: 题型:
![]()
(1)B的平衡浓度为__________。
(2)A的转化率为__________。
(3)用D表示的平均反应速率为__________。
(4)如果缩小容器容积_________(温度不变),则平衡体系中混合气体的密度、平均相对分子质量__________。(两空均填“增大“减少”或“不变”)
(5)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的体积分数与原平衡相等,则还应加入__________mol B物质。
查看答案和解析>>
科目: 来源: 题型:
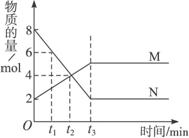
(1)该反应的化学方程式为________________________。
(2)t1时生成M反应速率_________ (填“大于”“小于”或“等于”)生成N的反应速率。
(3)达到平衡状态的时间为_________,此时N的转化率为_________。
(4)若生成M反应为吸热反应,在压强不变的情况下升高温度,容器的体积将_________ (填“增加”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
A.硫酸生产中常采用高压条件提高SO2的转化率
B.合成氨中采用及时分离氨气提高反应速率
C.电解精炼铜时,溶液中c(Cu2+)基本保持不变
D.铝热反应常用于冶炼某些熔点较低的金属
查看答案和解析>>
科目: 来源: 题型:
X(g)+Y(g)![]() 2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为
2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为

下列说法错误的是( )
A.反应速率:v(B)>v(A)
B.A容器中X的转化率为80%
C.平衡时的压强:p(B)>2p(A)
D.平衡时Y的体积分数:A>B
查看答案和解析>>
科目: 来源: 题型:
A.c1∶c2=1∶3
B.平衡时,Y和Z的生成速率之比2∶3
C.X和Y的转化率相等
D.c1的取值范围为0<c1<0.14
查看答案和解析>>
科目: 来源: 题型:
A.反应体系的总压恒定 B.B的浓度不变
C.c(A)∶c(B)=1∶3 D.2v正(B)=3v逆(C)
查看答案和解析>>
科目: 来源: 题型:

图Ⅰ 图Ⅱ
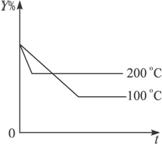
则下列结论正确的是( )
A.在t0时,其他条件不变,增大压强,平衡向逆反应方向移动
B.其他条件不变,升高温度,v(正)减小,v(逆)增大,平衡向逆反应方向移动
C.正反应为吸热反应
D.该反应的化学方程式为X+3Y![]() 2Z
2Z
查看答案和解析>>
科目: 来源: 题型:
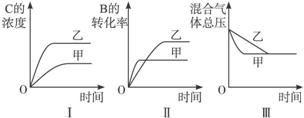
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅰ研究的是压强对反应的影响,且乙的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com