
科目: 来源: 题型:
Na2CO3·10H2O与NaHCO3混合物n g溶于水制成400 mL溶液中c(Na+) = 0.5 mol·L-1,若将n g该混合物加热到质量不变时,质量为
查看答案和解析>>
科目: 来源: 题型:
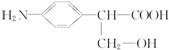
请回答:
(1)写出A的化学式:_______________________________________________。
(2)写出下列变化的基本反应类型:
A![]() C:____________________________________________________;
C:____________________________________________________;
E![]() F:____________________________________________________。
F:____________________________________________________。
(3)写出D的结构简式:____________________________________________________。
(4)B发生银镜反应的离子方程式_______________________________________。
(5)若E中的苯环和各官能团均保持不变,苯环上取代基的数目、位置和化学式也不改变。则符合上述条件的E的同分异构体(除E外)还有____________种。
查看答案和解析>>
科目: 来源: 题型:
在一个容积为![]()
![]() ,K为只与温度有关的常数。回答下列问题:
,K为只与温度有关的常数。回答下列问题:
(1)用B的浓度变化来表示的反应速率v(B)=___________,A的转化率为___________,该反应在此温度下的K=___________。
(2)在相同实验条件下,若在同一容器中加入2.0 mol A和8.0 mol B,若要求平衡后C在反应混合气中体积分数不变,则还应加入C___________mol。
(3)在相同实验条件下,若在同一容器中加入3.0 mol A和一定量的B,平衡时C的物质的量为3.0 mol,则加入的B的物质的量为___________mol。
查看答案和解析>>
科目: 来源: 题型:

(1)画出f元素的原子结构示意图_____________。在a、c、d三种元素形成的化合物中存在的化学键类型是_____________。
(2)写出d、e两元素的最高价氧化物的水化物之间反应的离子方程式________________。
(3)a、b、c三种元素的原子按照原子个数4∶1∶1组成化合物M,已知:
M(l)+O2(g)====CO(g)+2H2O(g) ΔH1=-443.6 kJ·mol-1
2CO (g)+O2(g)====2CO2(g) ΔH2=-566.0 kJ·mol-1
试写出M(l)完全燃烧〔生成H2O(g)〕的热化学方程式:______________________________。
(4)以M溶液、氧气为基本反应物的新型燃料电池已经问世,其结构如上图所示(甲醇电离出的H+,可以通过质子交换膜进入另一极)。请写出甲醇在电极上反应的方程式:________________________________,当有
(5)某同学以M燃料电池为电源,均以石墨为电极电解CuSO4溶液,则与电池正极相连的电解池电极上反应的方程式为____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)制取氧气
①用20%的H2O2溶液,通过反应2H2O2![]() 2H2O+O2↑来制取氧气,则在下列A、B、C三装置中最佳装置是_____________;
2H2O+O2↑来制取氧气,则在下列A、B、C三装置中最佳装置是_____________;
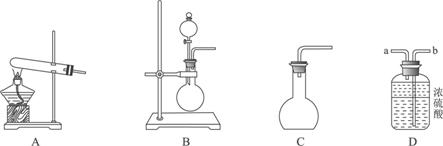
②与气体发生装置相连接的D装置的导管口是_____________;
③为了能使产生的氧气被充分干燥,可采取的操作是______________________________。
(2)制取氧化铜
将m g铜粉在氧气流中加热到高温,使铜粉全部氧化,得n g粉末X。乙同学查阅资料知:铜与氧气的反应有:①2Cu+O2![]() 2CuO,②4CuO
2CuO,②4CuO![]() 2Cu2O+O2↑;在酸性条件下:2Cu+(aq)====Cu(s)+Cu2+(aq)。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物并不一定是纯CuO,可能含有一定量的氧化亚铜(Cu2O)。
2Cu2O+O2↑;在酸性条件下:2Cu+(aq)====Cu(s)+Cu2+(aq)。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物并不一定是纯CuO,可能含有一定量的氧化亚铜(Cu2O)。
(3)探究铜的氧化物的成分
为测定粉末X中是否含有Cu2O,甲、乙、丙三同学分别设计如下实验方案。
甲同学的实验方案是:向粉末X中加入稀硫酸,若有_____________,则说明固体中含有Cu2O。
乙同学的实验方案是:再将粉末X放入氧气中加热,如果其质量增加,则说明其中含有Cu2O。
丙同学的实验方案是:通过分析实验数据就可以确定粉末X的成分。
若n的取值范围是__________≤n<__________,则粉末X中含有Cu2O,其物质的量是__________。
请你再设计一个与上述三个实验方案中现象不同的实验方案,通过对化学反应和对实验现象的分析来确定粉末X中是否含有Cu2O。写出该实验中离子反应的方程式。
查看答案和解析>>
科目: 来源: 题型:
A.CO2(g)+NaOH(aq)====NaHCO3(aq) ΔH=-(2y-x) kJ·mol-1
B.CO2(g)+NaOH(aq) ====NaHCO3(aq) ΔH=-(2x-y) kJ·mol-1
C.CO2(g)+NaOH(aq) ====NaHCO3(aq) ΔH=-(4x-y) kJ·mol-1
D.2CO2(g)+NaOH(l) ====NaHCO3(l) ΔH=-(8x-2y) kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.1 mol Cl2与足量铁反应转移的电子数是3NA
B.
C
D.标准状况下,
查看答案和解析>>
科目: 来源: 题型:
(1)软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4![]() MnSO4+ZnSO4+S+2H2O。
MnSO4+ZnSO4+S+2H2O。
(2)除去反应混合物中的不溶物。
(3)电解混合液MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4
下列说法不正确的是
A.步骤(1)中MnO2和H2SO4都是氧化剂
B.步骤(1)中每析出
C.电解时MnO2在阳极处产生
D.硫酸在生产中可循环使用
查看答案和解析>>
科目: 来源: 题型:
A.其中有硫元素 B.其中有金属元素
C.这三种元素能够组成盐 D.这三种元素均位于不同周期
查看答案和解析>>
科目: 来源: 题型:
A.c=![]() mol·L-1 B.w%=
mol·L-1 B.w%=![]() %
%
C.S=![]() D.c(Cl-)=
D.c(Cl-)=![]() mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com