
科目: 来源: 题型:

(1)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应①的化学方程式是______________________________。
(2)若B为一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D和E的循环。反应②的离子方程式是______________________________;在反应③中,若转移的电子数目为0.1 mol,则生成的D在标准状况下的体积为____________L。
(3)若反应①②③均为水溶液中的反应,A、D、E为ⅦA族元素的单质,则A、D、E的氧化性由强到弱的顺序为___________,其中A的化学式为___________。B、C、F呈固态时为___________(填“分子晶体”“离子晶体”或“原子晶体”),如B、C、F为气态氢化物时,则B、C、F分子的热稳定性由强到弱的顺序为___________。
查看答案和解析>>
科目: 来源: 题型:
①过滤 ②NaOH ③BaCl2 ④盐酸 ⑤Na2CO3
当电解
(2)摩托罗拉公司研发了一种由甲醇(CH3OH)和氧气以及强碱作电解质溶液的新型手机电池。若放电过程中,甲醇完全氧化产生的CO2被碱充分吸收生成![]() 。则该电池反应的总离子方程式为________________________________________;甲醇在_____________极发生_____________反应。
。则该电池反应的总离子方程式为________________________________________;甲醇在_____________极发生_____________反应。
查看答案和解析>>
科目: 来源: 题型:
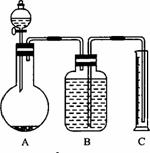
(1)甲组:中和滴定法
滴定时用到的主要试剂是:标准盐酸和_____________________________,用到的2件主要玻璃仪器是_______________________________。
(2)乙组:气体分析法
称取一定量的混合物与足量盐酸反应,用上图装置测定产生的CO2气体的体积,为减小CO2在B中溶液的溶解质量,B中应盛放_____________溶液,选用该溶液后实验结果可能不够精确,主要原因是________________________________________________________________
____________________________________________________________________。
(3)丙组:沉淀分析法
称取一定量的混合物溶解后加入过量CaCl2溶液,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是_________________________________________________
____________________________________________________________________。洗涤沉淀多次,检验沉淀是否洗净的操作是_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.进行中和热测定时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
B.用稀盐酸洗涤盛放过石灰水的试剂瓶
C.用洁净铂丝蘸取固体配制的溶液,置于酒精灯火焰上灼烧,火焰呈黄色,肯定无钾元素
D.欲量取20.00 mL溴的四氯化碳溶液,现取一支25 mL的碱式滴定管,先用溴的四氯化碳溶液润洗,再加溶液至1.00 mL处,用手挤压玻璃球,放溶液到21.00 mL处
E.检验红砖中的氧化铁成分时,在红砖粉末中加入稀盐酸,静置后取上层清液,再滴加2—3滴硫氰化钾溶液
F.氢气还原氧化铜实验中,先通氢气后加热氧化铜
G.用镊子取出白磷并置于水中切割
H.实验室做钠的实验时,余下的钠屑投入到废液缸中
I.中和滴定时,酸式滴定管用蒸馏水清洗3次后,再加入标准盐酸进行滴定
J.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
K.用冰醋酸、蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
查看答案和解析>>
科目: 来源: 题型:
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为2CuFeS2+4O2====Cu2S+3SO2+2FeO(炉渣)
(3)制粗铜,在1
2Cu2S+3O2====2Cu2O+2SO2;
2Cu2O+Cu2S====6Cu+SO2↑
(4)电解精炼
下列说法不正确的是
A.上述灼烧过程的尾气均不能直接排到空气中
B.由6 mol CuFeS2生成6 mol Cu,上述共消耗15 mol O2
C.在反应2Cu2O+Cu2S====6Cu+SO2↑中,作氧化剂的只有Cu2O
D.电解精炼时,粗铜应与外电源正极相连
查看答案和解析>>
科目: 来源: 题型:
A.向无色溶液中加氯水变橙色,溶液中可能含:![]() ,Br-,OH-,Ba2+
,Br-,OH-,Ba2+
B.在c(H+)=10-14 mol·L-1?的溶液中可能含:Na+,![]() ,
,![]() ,
,![]()
C.某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,![]()
D.使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ca2+,![]()
查看答案和解析>>
科目: 来源: 题型:
A.pH=4的盐酸和pH=10的氨水
B.pH=4的醋酸溶液和pH=10的氢氧化钾溶液
C.0.2 mol·L-1的盐酸和0.2 mol·L-1的氢氧化钾溶液
D.0.2 mol·L-1的盐酸和0.2 mol·L-1的氢氧化钡溶液
查看答案和解析>>
科目: 来源: 题型:
①As2O3是砷的最高价含氧酸的酸酐
②可向河水中投入纯碱,以消除对河水的污染
③As2O3的晶体为分子晶体
④可向河水中撒入生石灰,以消除对河水的污染
A.①② B.②③ C.①④ D.③④
查看答案和解析>>
科目: 来源: 题型:
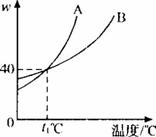
A.t
B.t
C.t
D.t
查看答案和解析>>
科目: 来源: 题型:
A.依据元素的原子结构,可以推知其在元素周期表中的位置
B.依据沸点的数据,判断将两种互溶的液态混合物用蒸馏方法分离开来的可能性
C.依据相对分子质量,一定能判断组成和结构相似的物质熔、沸点的高低
D.依据中和热的数据,推算一定量的H2SO4和NaOH的两种稀溶液反应放出的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com