
科目: 来源: 题型:
①鸡蛋清溶液遇浓硝酸→黄色 ②淀粉溶液遇单质碘→蓝色?③溴化银见光分解→白色 ④热的氧化铜遇乙醇→黑色 ⑤新制氯水久置后→无色 ⑥苯酚在空气中氧化→粉红色
A.①②③⑤ B.②④⑤
C.①②⑤⑥ D.②③⑥
查看答案和解析>>
科目: 来源: 题型:
A.用铜片作阴、阳电极,电解硫酸锌溶液
B.铜片作原电池的负极,碳棒作原电池的正极,氯化锌作电解质溶液
C.铜锌合金在潮湿空气中发生电化学腐蚀
D.用锌片作阴、阳电极,电解硫酸铜溶液
查看答案和解析>>
科目: 来源: 题型:
A.使用农家肥导致粮食、蔬菜不清洁
B.农村目前使用农作物的禾秆作燃料产生大量二氧化碳造成温室效应
C.工业生产中向食品中加入适量的防腐剂造成食品污染
D.排放含有机和含磷洗衣粉污水的城市生活小区,造成水质污染
查看答案和解析>>
科目: 来源: 题型:
(1)盐酸中HCl的物质的量浓度。
(2)取上述所得盐酸体积的十分之一跟足量的锌粒反应,在
查看答案和解析>>
科目: 来源: 题型:
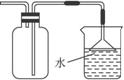
化学试剂:①NH4Cl固体、②浓氨水、③固体 NaOH
(1)甲同学想方便快速制取少量氨气,应选择的装置是__________(填序号)。选用试剂是__________(填序号),选用上述试剂制氨气的理由是__________________________________。实验过程中,制气时的实验操作是_____________________________________________。
(2)乙同学建议,把教材中实验室制取氨气的收集装置由大试管改为集气瓶且瓶口向上收集氨气,并确保不污染环境,请你根据其设想回答:
①若用排气法收集氨气,请在图Ⅱ的方框内画出其气体收集装置和尾气吸收装置,标出所用试剂(自选)名称。
②若用排液集气法收集NH3,可选用的试剂是__________(填序号)。
A.H2O B.浓H2SO
查看答案和解析>>
科目: 来源: 题型:
丙烯![]()
![]() 1,2,3-三氯丙烷(ClCH2CHClCH2Cl)
1,2,3-三氯丙烷(ClCH2CHClCH2Cl)![]()
![]() 硝化甘油
硝化甘油
已知:CH2CHCH3+Cl2![]() ClCH2CHClCH3
ClCH2CHClCH3
CH2CHCH3+Cl2![]() CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
(1)写出③、④各步反应的化学方程式,并分别注明其反应类型:
③________________________,( )。
④________________________,( )。
(2)请写出用正丙醇作原料,制丙烯的反应的化学方程式___________________________。
(3)如果所用正丙醇中混有异丙醇〔CH3CH(OH)CH3〕,对所制丙烯的纯度是否有影响,简要说明理由__________________________________________。
查看答案和解析>>
科目: 来源: 题型:

(1)写出E的电子式:____________。
(2)写出反应⑦的离子方程式:______________________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:_____________________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:______________________________。____________极(填“阴”或“阳”)附近溶液由无色变为红色,其原因是_______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)我国目前多用煅烧黄铁矿的方法来制备二氧化硫,该反应的化学方程式为___________
________________________________,该反应常在______________________(填写设备名称)内进行。

(2)现有A、B、C、D四地的地理位置如图所示,交通均较为便利,其他地理条件如下:A地是风景旅游城市;B地是硫酸消费中心;C地有较为丰实的黄铁矿资源;D地有少量的硫酸消费。则硫酸工厂厂址应选择在___________地。
(3)如果某厂生产98%的浓硫酸100 t,在生产过程中硫的总损耗率为2%,则需要含FeS260%的黄铁矿____________t。
查看答案和解析>>
科目: 来源: 题型:
(1)写出该燃料电池总的化学反应方程式___________________________________。
(2)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,为此,必须在正极通入的空气中加入一种物质,其加入的物质是(写化学式)________________;它从哪里来?从___________来。
查看答案和解析>>
科目: 来源: 题型:

(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是_______________。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是___________(填名称),可以验证该结论的实验是___________。(填序号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com