
科目: 来源: 题型:
| 实验事实 | 结论 |
A | NH3的水溶液可以导电 | NH3是电解质 |
B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
C | Ca(ClO)2溶液中通入CO2产生白色沉淀 | 酸性:H2CO3>HClO |
D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
查看答案和解析>>
科目: 来源: 题型:
A.①②⑤ B.②③⑥ C.①②③ D.④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
(1)充分加热后,剩余固体重______________ g。
(2)该天然碱成分中除含有碳酸钠外,还含有______________(填化学式)。
(3)6.64 g天然碱中,含碳酸钠的物质的量为______________mol。
(4)该天然碱的化学式为_________________________。
查看答案和解析>>
科目: 来源: 题型:

Ⅰ
(1)实验前应先检验装置的气密性,方法是_______________________________________。
(2)实验室用亚硫酸钠固体与硫酸反应制取SO2气体,写出该反应的化学方程式__________________________________。
(3)分别将SO2气体通入下列C溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是_______________________,继续通入过量的SO2气体,现象是__________________________。
②SO2通入紫红色KMnO4溶液,现象是__________________________,写出反应的离子方程式__________________________。
③SO2慢慢通入(可以1个气泡1个气泡地通入)澄清石灰水中,现象是_______________。
④SO2通入少量的澄清石灰水中,没有明显现象,原因是_____________________________。
(4)若该同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。
![]()
Ⅱ
可以选择图Ⅱ洗气装置设计实验。洗气装置里的溶液是:A.浓硫酸、B.氢氧化钠溶液、C.硫酸铜溶液、D.品红溶液、E.澄清石灰水、F.高锰酸钾溶液、G.碳酸氢钠溶液。
上述装置的连接顺序是______________。(用字母表示,所给装置可以重复使用,有些装置也可以不用)。?
查看答案和解析>>
科目: 来源: 题型:
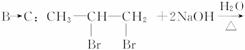 。又知A为烃,在一定条件下两个E分子之间缩合可生成六元环状化合物,H为高分子化合物,相关物质转化关系如下图:
。又知A为烃,在一定条件下两个E分子之间缩合可生成六元环状化合物,H为高分子化合物,相关物质转化关系如下图: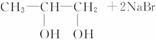
(1)以上反应中,属于取代反应的有________(填序号,下同),属于消去反应的有__________。
(2)写出下列物质的结构简式:
D_______________________,F_______________________。
(3)写出下列反应的化学方程式:
B→C______________________________;G→H______________________________。
查看答案和解析>>
科目: 来源: 题型:
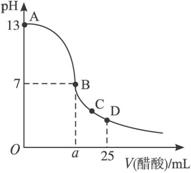
(1)写出氢氧化钠溶液与醋酸溶液反应的离子方程式:__________________________。
(2)该氢氧化钠溶液的物质的量浓度为_____________mol·L-1。
(3)在B点,a_____________12.5 mL(填“大于”“小于”或“等于”,下同)。若由体积相等的氢氧化钠和醋酸溶液混合而且恰好呈中性,则混合前c(NaOH)____________c(CH3COOH),混合前酸中c(H+)和碱中c(OH-)的关系:c(H+)_____________c(OH-)。
(4)在D点,溶液中离子浓度大小关系为_____________。
查看答案和解析>>
科目: 来源: 题型:
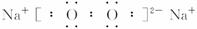
(1)A的分子式是___________,甲的电子式是___________。
(2)D的溶液与乙反应的离子方程式是__________________________。
(3)若1.7 g A与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式:_______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
信息 | 问题 |
①短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数均不少于最内层电子数。其中X是形成化合物种类最多的元素 | (1)X的最高价氧化物的电子式为_______________ |
②在一定条件下,上述四种元素的单质均能与足量的氧气反应,其中Z元素的氧化物既能溶于稀硫酸,又能溶于浓NaOH溶液 | (2)Z元素在元素周期表中位于第_________周期,_________族 |
③Y固体单质与盐酸反应,再向反应后的溶液中加入过量的烧碱溶液,最终溶液中有白色沉淀生成 | (3)写出生成白色沉淀的化学方程式_________________________ _____________________________ |
④向上述四种元素的单质的混合物中,加入足量的烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸溶液,最终溶液中有白色沉淀生成 | (4)最终生成白色沉淀的离子方程式为_______________________ _____________________________ |
(5)X、Y、Z、W四种元素的原子半径由大到小的顺序为__________(用元素符号表示) | |
查看答案和解析>>
科目: 来源: 题型:
A.氢元素被氧化,碳元素被还原 B.HCN既是氧化剂又是还原剂
C.CaCN2是还原产物,H2是氧化产物 D.CO是氧化产物,H2是还原产物
查看答案和解析>>
科目: 来源: 题型:
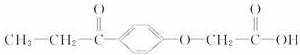
下列叙述正确的是
A.1 mol利尿酸最多可与5 mol H2发生加成反应
B.利尿酸分子中位于同一平面内的原子有10个
C.利尿酸分子式是C11H12O4
D.利尿酸与新制Cu(OH)2悬浊液反应有红色沉淀生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com