
科目: 来源: 题型:
A.加入(NH4)2Fe(SO4)2·6H2O晶体后的溶液中:K+、H+、Cl-、![]()
B.水电离产生的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、ClO-、I-
C.![]() =10-10的溶液中:Na+、
=10-10的溶液中:Na+、![]() 、Br-、
、Br-、![]()
D.能和铝反应产生氢气的溶液中:K+、Mg2+、Cl-、![]()
查看答案和解析>>
科目: 来源: 题型:
A.某水溶液中加入盐酸酸化的Ba(NO3)2溶液,出现白色沉淀,则原溶液中一定存在![]()
B.用过滤的方法分离水和少量苯酚的混合物
C.把装有NO2和N2O4混合气体的烧瓶,放入到热水中,混合气体的颜色将变浅
D.硫酸铜晶体结晶水测定实验中,盛硫酸铜晶体的坩埚加热后,要放在干燥器内冷却后再称量
查看答案和解析>>
科目: 来源: 题型:
A.铀的某种同位素![]() ,其中子数与质子数之差为143
,其中子数与质子数之差为143
B.在周期表中,元素种类最多的族为ⅢB
C.最外层有6个电子的原子都是非金属原子
D.同主族元素,原子序数越大,其单质与水的反应越容易
查看答案和解析>>
科目: 来源: 题型:
A.石英、水晶、人造刚玉、光导纤维等物质的主要成分是SiO2
B.工业制硫酸过程中为了提高吸收效率,用98.3%的浓硫酸来吸收SO3
C.用聚氯乙烯塑料制作炒锅手柄
D.工业上为了加快分离胶体中的电解质杂质,常在渗析袋外施加电场,使电解质离子透过半透膜向两极移动,该操作是应用胶体的电泳原理
查看答案和解析>>
科目: 来源: 题型:
①量取25.00 mL甲溶液,向其中缓慢滴加乙溶液15.00 mL,共收集到二氧化碳气体224 mL。
②另取15.00 mL乙溶液,向其中缓慢滴加甲溶液25.00 mL,共收集到二氧化碳气体112 mL。
上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:
(1)写出上述过程中所涉及反应的离子方程式:①_______________;②______________;③______________。
(2)甲是______________,甲溶液的物质的量浓度为______________,乙溶液的物质的量浓度为______________。(二氧化碳在溶液中的少量溶解忽略不计)
(3)将n mL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体积为V mL(标准状况),则V的取值范围为____________________。
查看答案和解析>>
科目: 来源: 题型:

(1)B单质的化学式为______________,丙的化学式为______________。
(2)判断A和C的还原性的强弱,A________C(填“>”“<”)。
(3)写出D与烧碱溶液反应的化学方程式:______________________________________。
(4)写出甲和D反应的化学方程式:____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C同周期。
(2)W由A、B组成,其分子中原子个数比为A∶B=4∶1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A∶C=1∶1。
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1∶1。
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2∶1,则
(a)B的元素符号为______________,写出三种B的不同单质(写名称)_____________、____________、____________;
(b)W化学式为____________,其分子的空间构型名称为____________;
(c)X的结构式为____________,属于____________分子(填极性或非极性);
(d)Y的电子式为____________,属于____________晶体。
(e)Z的水溶液呈____________性,原因是(用离子方程式表示)___________________。
查看答案和解析>>
科目: 来源: 题型:
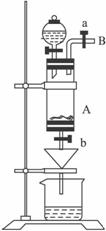
(1)滴加盐酸时,发现反应速率比盐酸与纯铁粉的反应快,其原因是_________________。
(2)烧杯中稀HNO3的作用是(用离子方程式表示)_______________________________。
(3)整个实验过程中,弹簧夹a必须始终打开,其目的是___________________________。
(4)若不用降温结晶的方法制取FeCl3·6H2O,而是直接将溶液蒸干,则此时得到的固体是____________(写化学式)。
(5)把制得的FeCl3·6H2O适量放入水中配成浓溶液,取少量滴入沸水中,可以得到一种红褐色的透明的分散系。写出有关的化学方程式:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.89.6 mL B.112 mL C.168 mL D.224 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com