
科目: 来源: 题型:
A.碳酸钙溶于醋酸CaCO3+2H+====Ca2++CO2↑+H2O
B.等体积、等物质的量浓度的氢氧化钡与硫酸氢钠溶液混合Ba2++2OH-+2H++![]() ==== BaSO4↓+2H2O
==== BaSO4↓+2H2O
C.铜溶于稀硝酸中Cu+4H++2![]() ====Cu2++2NO2↑+2H2O
====Cu2++2NO2↑+2H2O
D.漂白粉溶液中通入少量二氧化碳气体Ca2++2ClO-+CO2+H2O====CaCO3↓+2HClO
查看答案和解析>>
科目: 来源: 题型:
A.在原子晶体中可能存在极性共价键
B.在离子晶体中可能存在非极性共价键
C.含有阳离子的晶体中,不一定含有阴离子
D.在分子晶体中一定含有共价键
查看答案和解析>>
科目: 来源: 题型:
A.位于第七周期第ⅦA族 B.具有“两性”
C.原子核外共有6个电子层 D.该原子中,中子数与质子数之差为43
查看答案和解析>>
科目: 来源: 题型:
N2(g)+3H2(g)![]() 2NH3(g);ΔH<0
2NH3(g);ΔH<0
当反应达到平衡后,分离出氨,并补充氮气、氢气物质的量之比与起始时相同的原料气,以实现连续的生产,各组分物质的量和时间的关系见下图。
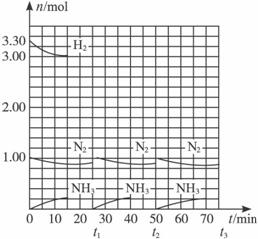
(1)起始时刻氮气与氢气的物质的量之比n(N2)∶n(H2)=___________。反应开始至15 min时第一次达到平衡,容器体积为
(2)写出代表H2的曲线在下列时刻的坐标:
t1补充原料气之后:(_________,_________),t2处于平衡态时:(_________,_________)。
在图上画出t1—t2间的曲线。
(3)第一次达平衡时H2的转化率是___________。以t1补充原料气之后为起始状态,第二次达平衡时H2的转化率是___________。
以这样的氮气和氢气的物质的量之比补充原料气,经济上是否合算?___________。
查看答案和解析>>
科目: 来源: 题型:
(2)联氨是一种可燃性液体,可用作火箭燃料。已知32.0 gN2H4和H2O2反应生成氮气和水(气态),放出热量642 kJ,该反应的热化学方程式是:_____________________________。
(3)联氨—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。联氨—空气燃料电池放电生成N2和H2O,其电极反应式是:
正极:_____________________________________________________________;
负极:______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
①E和K为无色气体单质,F为常见的金属,它在高温下与某些金属氧化物反应是工业上冶炼金属的方法之一。
②A为无色气体,B为淡黄色固体,C为无色液体。
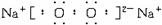
(1)写出以下物质的化学式:
A______________,H______________,I______________。
(2)写出B的电子式______________,固态G属于______________晶体。
(3)写出F+G+C![]() J+K的化学方程式:________________________。
J+K的化学方程式:________________________。
查看答案和解析>>
科目: 来源: 题型:
CuSO4![]() CuO+SO3↑ 2SO3
CuO+SO3↑ 2SO3![]() 2SO2↑+O2↑某研究性学习小组设计了下图所示装置(夹持仪器已略去),利用D管在反应前后的质量差计算分解的无水CuSO4的质量。
2SO2↑+O2↑某研究性学习小组设计了下图所示装置(夹持仪器已略去),利用D管在反应前后的质量差计算分解的无水CuSO4的质量。

实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一定时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的空气。
④再称量D管,得其反应前后的质量差为m。
(1)B管中出现的现象是_________________________________________________。
有关离子方程式是______________________________________________________。
(2)B管的作用是除去混合气体中的SO3,实验过程中发现B管的温度明显升高,主要原因是____________________________________________________________________。
(3)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算分解的无水CuSO4的质量?__________(填“能”或“不能”),原因是________
_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
A.CuSO4 B.Na2SO
查看答案和解析>>
科目: 来源: 题型:
A.![]() +H2O
+H2O![]()
![]() +OH- B.
+OH- B.![]() +H2O
+H2O![]() H2SO3+OH-
H2SO3+OH-
C.![]() +OH-====
+OH-====![]() +H2O D.H2SO3+OH-====
+H2O D.H2SO3+OH-====![]() +H2O
+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com