
科目: 来源: 题型:
Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.
2Na2S2O3+I2=Na2S4O6+2NaI
滴定时用去Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
查看答案和解析>>
科目: 来源: 题型:
(1)x、y、z为整数,且x+y+z=7。
(2)取8.
(3)发生上述反应后,A、D以阳离子存在于溶液中。往溶液里加入过量的铁粉,其中使D离子全部还原所消耗的铁粉质量为0.
(4)化合物中D元素的质量分数为12.8%。
试通过计算和推理确定E、G、D、A各是什么元素,求出x、y、z的值,并写出该化合物的分子式。
解:(1)确定E和G:E是_______________;G是________________。
(2)确定x、y、z和D:
x=____________,y=____________,z=____________;D是____________。
(3)确定A并写出化合物的分子式:
A是____________;该化合物的分子式是____________。
查看答案和解析>>
科目: 来源: 题型:
已知:
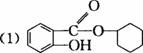

图8-7
(1)写出C的结构简式:___________________________。
(2)写出反应②的化学方程式:__________________________________。
(3)写出G的结构简式:_________________。
(4)写出反应⑧的化学方程式:__________________________________。
(5)写出反应类型:④_________________,⑦_________________。
(6)下列可检验阿司匹林样品中混有水杨酸的试剂是_________________。
(a)三氯化铁溶液 (b)碳酸氢钠溶液 (c)石蕊试液
查看答案和解析>>
科目: 来源: 题型:
 可简写为
可简写为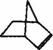
(1)降冰片烯属于__________________。
A.环烃 B.不饱和烃 C.烷烃 D.芳香烃
(2)降冰片烯的分子式为_________________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为_____________。
(4)降冰片烯不具有的性质为______________。
A.能溶于水 B.能发生氧化反应 C.能发生加成反应 D.常温常压下为气体
查看答案和解析>>
科目: 来源: 题型:

图8-6
请填空:
(1)形成单质A的原子的结构示意图为_______________,它的最高化合价为___________。
(2)B的化学式(分子式)为___________,B的晶体类型为___________。
B和碳反应生成A和E的化学方程式是_________________。
(3)C的化学式(分子式)为____________,D的化学式(分子式)为_____________。
查看答案和解析>>
科目: 来源: 题型:

图8-5
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式:
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:
(3)容器c中NaOH溶液的作用是:
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗的乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因:
查看答案和解析>>
科目: 来源: 题型:
![]()
请回答:
(1)W的电子式是_________________。
(2)X与Y在溶液中反应的离子方程式是___________________________。
(3)X含有的四种元素之间(两种、三种或四种)可组成多种化合物,选用其中某些化合物,利用图8-4所示装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。①装置I中反应的化学方程式是_________________。装置Ⅱ中物质的化学式是_________________。

图8-4
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下,直接制备并收集纯净干燥的装置V中气体,该化合物的化学式是________________________,所需仪器装置是_______________(从上图选择必要的装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是___________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
甲:①称取一定质量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的一种定量仪器是_________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH_________1(选填“>”、“<”或“=”)
乙方案中,说明HA是弱电解质的现象是__________。
(a)装HCl溶液的试管中放出H2的速率快
(b)装HA溶液的试管中放出H2的速率快
(c)两个试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现之处和不妥之处是__________________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要的表述。
查看答案和解析>>
科目: 来源: 题型:
2H2O(g)![]() 2H2+O2;2CO+O2
2H2+O2;2CO+O2![]() 2CO2。
2CO2。
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是_________和_________,或________和________。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为n(O2)平=amol,n(CO2)平=bmol。试求n(H2O)平=_____________。(用含a、b的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
(1)不能使品红试液褪色,说明该气体中不含_____________(填分子式)。
(2)此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母):
第一种情况是_______________________;第二种情况是_______________________;
第三种情况是_______________________;第四种情况是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com