
科目: 来源: 题型:
A.明矾净水过程中不涉及化学变化
B.由同种元素组成的物质一定是纯净物
C.风化、石油分馏和碘的升华都是物理变化
D.在化学反应中,反应前后原子种类、数目和质量一定不变
查看答案和解析>>
科目: 来源: 题型:
A.“可燃冰”是将水变为油的新型燃料
B.氢气是具有热值高、无污染等优点的燃料
C.乙醇是比汽油更环保、不可再生的燃料
D.石油和煤是工厂经常使用可再生的化石燃料
查看答案和解析>>
科目: 来源: 题型:
(1)试求稀释后溶液的pH。
(2)求生成的气体中NO2和NO的物质的量(可以含有B的代数式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO2+2NaOH=2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,试讨论B的取值范围。
查看答案和解析>>
科目: 来源: 题型:
实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
1 | 0.858 | 0.5 | 1.379 |
2 | 1.716 | 0.5 |
|
3 | 2.574 | 0.5 | 4.137 |
4 | 3.432 | 0.5 | 5.516 |
5 | 4.290 | 0.5 | 5.516 |
6 | 5.148 | 0.5 | 5.516 |
请回答下列问题:
(1)第二次实验中产生沉淀的质量是_____________g。
(2)混合物中K2CO3和NaHCO3的物质的量之比为_____________。
(3)在![]() ,加水配成500mL溶液,求此溶液的pH(要求写出计算过程)。
,加水配成500mL溶液,求此溶液的pH(要求写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
![]() (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)
![]()
下面是PAS—Na的一种合成路线(部分反应的条件未注明):
请按要求回答问题:
(1)写出下列反应的化学方程式并配平:
A→B:____________________________________________;
B→C7H6BrNO2:____________________________________;
(2)写出下列物质的结构简式:C:____________D:____________;
(3)指出反应类型:Ⅰ____________,Ⅱ____________;
(4)指出所加试剂名称:X____________,Y____________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某医学杂质上用图11-9表示甲、乙两种物质的结构简式,这两种结构简式虽不是很符合有机物结构简式的书写规范,但还是能够清楚地表示甲、乙两种物质的结构特征。
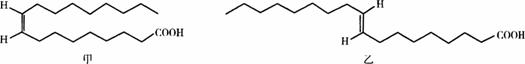
图11-9
请根据你所学过的化学知识回答下列问题:
(1)写出甲的分子式___________,甲和乙可互称为___________(填“同系物”或“同分异构体”)。你认为甲、乙两种哪一种是反式脂肪酸?___________。
(2)你认为甲、乙两种物质能否在空气中燃烧?___________,若你认为能够燃烧,请写出甲在足量氧气中燃烧的化学方程式:_________________________________。
(3)顺式脂肪酸多为液态,空间呈弯曲状,反式脂肪酸多为固态,空间呈线型。血液中反式脂肪酸含量过高,易使溶液堵塞血管而导致心脑血管疾病。原因是_________________________。
(4)在油脂催化氢化(如制备人造奶油、酥油)过程中,构型会发生变化。另外,油脂长时间高温加热,也会产生反式脂肪酸。若ag甲转化成乙吸收QkJ热量,写出该热化学反应方程式:___________(用“甲”、“乙”表示物质分子式)。
查看答案和解析>>
科目: 来源: 题型:
(1)单质F是_______________。
(2)写出由E生成G的离子反应方程式(或化学方程式)_________________________________。
(3)溶液I中所含金属离子是______________________。
(4)由C制取E时若改用浓酸,则不能选用的浓酸是(写分子式)_______________ ___________。
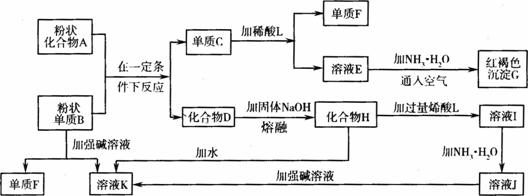
图11-8
查看答案和解析>>
科目: 来源: 题型:
(1)Na2O2、K2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最合适的过氧化物是___________。
(2)过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:_________________________________________。
(3)与过氧化氢具有相同电子总数且属于非极性分子的有___________、___________(举两例,写化学式)。
(4)纯的过氧化氢常用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态过氧化氢反应,生成N2和H2O(g),放出256.6kJ的热量。则该反应的热化学方程式为_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
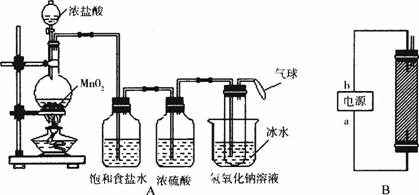
图11-7
请回答下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式:_______________________________________。
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的?__________(填“能”或“不能”)。
(3)装置A中盛冰水的烧杯的作用是____________________________________________。
(4)装置B制备消毒液时有关反应的化学方程式为_________________________________。
(5)a端应接电源的__________极,理由是____________________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
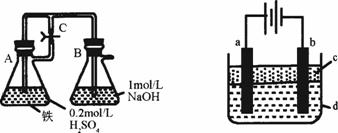
图11-5 图11-6
方法一:按照图11-5进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行。最终在___________容器中观察到白色沉淀,该实验中涉及到的化学方程式有__________________________。
方法二:按图11-6进行实验,最终在两极间的溶液中首先观察到白色沉淀。请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl2溶液 ⑥乙醇 ⑦Fe棒 ⑧植物油 ⑨碳棒
a为___________,b为___________,C为___________,d为___________。(填序号)
【探究思考】实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
资料名称 | 物理性质描述 | 化学性质描述 |
《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触时易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
《大学普通化学》(下册)傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3。这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+ |
阅读该资料后,你对上述实验中出现灰绿色或绿色的现象的解释是______________________;
资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成___________。
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2·nH2O所致。用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀有由绿变白的趋势。加热时,“方法一”中弹簧夹C应处于__________(填“打开”或“关闭”)状态,容器A中的反应需处于___________(填“停止”或“发生”)状态。
写出该实验中支持乙同学观点的化学方程式:______________________。
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com