
科目: 来源: 题型:
A.Mg2+、![]() 、Cl-、Na+ B.K+、Cl-、
、Cl-、Na+ B.K+、Cl-、![]() 、
、![]()
C.Na+、Cl-、![]() 、
、![]() D.Fe2+、
D.Fe2+、![]() 、I-、
、I-、![]()
查看答案和解析>>
科目: 来源: 题型:
c(Cl-)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.0.1 mol·L-1的醋酸溶液中:c(H+)=c(CH3COO-)
C.0.1 mol·L-1的硫化钠溶液中:c(Na+)=
D.将氨气通入一定量硫酸溶液中,充分反应后溶液pH=7,则:c(![]() )>c(
)>c(![]() )
)
查看答案和解析>>
科目: 来源: 题型:
①C17H35COOH ②C17H33COOH ③C15H31COOH ④C17H31COOH ⑤C17H29COOH
A.②④⑤ B.③②④ C.②③④ D.①⑤③
查看答案和解析>>
科目: 来源: 题型:
A.H2SO4(浓)+C B.Fe2O3+Al
C.Cl2+Mg D.NO2+H2O
查看答案和解析>>
科目: 来源: 题型:
A.原电池的正极和电解池的阳极均发生氧化反应
B.铜的电解精炼时,粗铜板作阳极
C.铜、锌和稀硫酸构成的原电池中铜为负极
D.石墨作电极电解氯化镁溶液的离子方程式为2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
A
B.pH=2、体积为
C.
D.标准状况下,
查看答案和解析>>
科目: 来源: 题型:
A.目前已被使用的高性能通信材料光导纤维的主要原料是硅
B.在医疗上,碳酸钠是治疗胃酸过多症的一种药剂
C.从电影业、照相业、科研单位和医院X光室回收的定影液中可以提取银
D.空气中的二氧化碳是造成光化学烟雾的主要因素
查看答案和解析>>
科目: 来源: 题型:
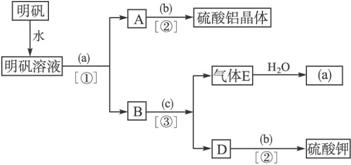
分析图中圆括号内应填入何种试剂,使用何种分离方法,并回答下列问题。
(1)试剂a是_____________,b是_____________,c是_____________,分离方法①是_____________,②是_____________,③是_____________。
(2)用离子反应方程式表示下列转化过程:
明矾溶液+a![]() A+B:_____________。B+C
A+B:_____________。B+C![]() E:_____________。
E:_____________。
(3)按上述操作不考虑损耗在理论上
查看答案和解析>>
科目: 来源: 题型:
实验步骤 | 实验内容 |
① | X与足量的金属钠反应产生氢气 |
② | X与醇或羧酸在浓硫酸加热条件下均能生成有水果香味的有机物 |
③ | 在一定条件下X的分子内脱水产物(不是环状化合物)可与溴水发生加成反应 |
④ |
(1)X的可能结构简式Ⅰ:______________,Ⅱ:______________,Ⅲ:______________。
(2)写出X发生①反应的化学方程式(任写一个):____________________________。
(3)在一定条件下有机物X可发生化学反应的类型有(填序号)______________。
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
(4)下列物质与X互为同系物的是(填序号)______________,与X互为同分异构体的是(填序号)______________。

(5)写出X与O2在铜作催化剂加热的条件下发生反应所得到的所有可能产物的结构简式:_____________。
查看答案和解析>>
科目: 来源: 题型:
(1)Y的元素符号是___________________。
(2)XW的电子式是________________。
(3)XW与YX3反应生成一种盐,该盐水溶液的pH_______________7(填“大于”“小于”或“等于”),其原因是(用离子方程式表示)___________________。
(4)Z元素氢化物的沸点比H2O_______________(填“低”或“高”)。Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式________________。
(5)已知X单质和Y单质反应生成YX3是可逆反应,ΔH<0。将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的是_________________。
a.达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,YX3的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com