
科目: 来源: 题型:
A.氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产方法又称“阳离子交换膜法”
B.生产普通玻璃的主要原料及设备:石灰石、石英、纯碱及玻璃熔炉
C.由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件
D.合成氨的反应是放热反应,因此工业合成常采用低温条件
查看答案和解析>>
科目: 来源: 题型:
A.从沸腾炉出来的炉气需净化,因为炉气中SO2会与杂质反应
B.硫铁矿燃烧前需要粉碎,因为大块的不能燃烧
C.SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以便使SO3吸收完全
D.SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率
查看答案和解析>>
科目: 来源: 题型:
A.3∶2 B.1∶2 C.1∶3 D.2∶3
查看答案和解析>>
科目: 来源: 题型:
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
A.1∶3 B.3∶2 C.6∶5 D.4∶3
查看答案和解析>>
科目: 来源: 题型:
| 200 atm | 600 atm |
500 ℃ | 19.1 | 42.2 |
而实际从合成塔出来的混合气体中含氨约为15%,这表明( )
A.表中所测数据有明显误差 B.生产条件控制不当
C.氨的分解速率大于预测值 D.合成塔中的反应并未达到平衡
查看答案和解析>>
科目: 来源: 题型:
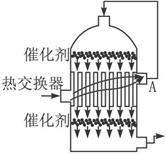
A.SO2 B.SO3、O2 C.SO2、O2 D.SO2、SO3
查看答案和解析>>
科目: 来源: 题型:
(1)按反应式2SO2+O2![]() 2SO3,SO2与O2的物质的量之比为2∶1,资料中却用1∶50,原因是:___________________________________________________________________。
2SO3,SO2与O2的物质的量之比为2∶1,资料中却用1∶50,原因是:___________________________________________________________________。
(2)进行冷却的原因是______________________________________________________。
(3)某工厂废气中含0.4%的SO2和0.5%的O2,你认为应该怎样利用上述资料?
(4)如果该工厂没有NH3,只有生石灰,你认为又该怎样利用上述资料?
(5)若将SO2全部转化为SO3,SO3全部转化为(NH4)2SO4,则资料中NH3的每小时通入量至少应是_________L,由此可得出NH3的利用率为_________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com