
科目: 来源: 题型:
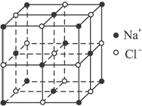
如图,直线交点处的圆圈为NaCl晶体中Na+和Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。
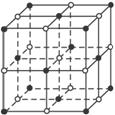
(1)请将其中代表Na+的圆圈涂黑(不考虑体积大小),以完成NaCl晶体结构示意图。
(2)晶体中,在每个Na+周围与它最接近的且距离相等的Na+共有( )
A.4个 B.6个 C.8个 D.12个
(3)晶体中,与每个Na+距离相等且距离最近的n个Cl-所围成的空间几何构型为( )
A.正四面体 B.正六面体
C.正八面体 D.正二十面体
(4)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶点上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于________个,即________(填计算式),Na+的个数等于___________,即________________________________(填计算式)。
(5)设NaCl的摩尔质量为M g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的Na+中心的距离为___________cm。
查看答案和解析>>
科目: 来源: 题型:
A.CH4·6H2O B.CH4·8H2O
C.CH4·10H2O D.CH4·14H2O
(2)“冰甲烷”中水分子与甲烷分子以___________相结合形成___________晶体。
(3)由于无水醋酸钠与碱石灰共热可以制得甲烷,你预测将无水苯乙酸钠与碱石灰共热时,所得的有机物主要是___________(填选项的字母)。
A.甲烷 B.甲苯 C.苯甲酸钠、甲烷 D.乙苯
(4)将甲烷分子的4个氢原子互相连接可以构成一个正四面体。如图所示是一个正立方体,设想将一个甲烷分子放入,碳原子将居于正立方体的中心,黑球表示已有1个氢原子居于该立方体的一角,请在图上画上另外三个黑球标出其他3个氢原子的位置。
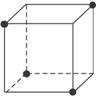
查看答案和解析>>
科目: 来源: 题型:
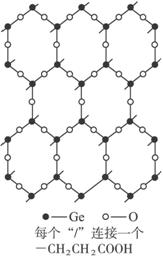
(1)每个正六边形拥有_________个锗原子,_________个氧原子。
(2)试写出Ge-132的化学式:___________________________。
查看答案和解析>>
科目: 来源: 题型:
| MgO | Al2O3 | MgCl2 | AlCl3 |
熔点/ ℃ | 2 852 | 2 072 | 714 | 190(2.5×105Pa) |
沸点/ ℃ | 3 600 | 2 980 | 1 412 | 182.7 |
请参考上述数据完成下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁,也不用电解AlCl3的方法生产铝?
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是_________________
_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
| 金刚石 | 晶体硅 | 晶体硼 |
熔点/K | 3 823 | 1 683 | 2 573 |
沸点/K | 5 100 | 2 628 | 2 823 |
硬度/moh | 10 | 7.0 | 9.5 |
(1)晶体硼的晶体类型属于__________晶体。
(2)已知晶体硼的基本结构单元是由硼原子构成的正二十面体(如图所示),其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子,通过观察图形及推算,可知此结构单元是由________个硼原子构成,其中B—B键间的键角是_________(填度数)。
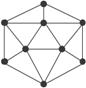
查看答案和解析>>
科目: 来源: 题型:
A.在晶体中只要有阴离子就一定有阳离子
B.在晶体中只要有阳离子就一定有阴离子
C.原子晶体的熔点一定比金属晶体的高
D.分子晶体的熔点一定比金属晶体的低
查看答案和解析>>
科目: 来源: 题型:
A.碳、氮原子构成网状结构的晶体
B.碳氮键比金刚石中的碳碳键更强
C.氮原子最外层电子数比碳原子最外层电子数多
D.碳氮单质的化学性质均不活泼
查看答案和解析>>
科目: 来源: 题型:
A.7∶8 B.13∶14 C.25∶25 D.26∶27
查看答案和解析>>
科目: 来源: 题型:
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质B |
熔点/ ℃ | 810 | 710 | 180 | 68 | 2 300 |
沸点/ ℃ | 1 465 | 1 418 | 160 | 57 | 2 500 |
A.SiCl4是分子晶体 B.单质B可能是原子晶体
C.AlCl3加热能升华 D.NaCl的键的强度比MgCl2小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com