
科目: 来源: 题型:
A.等于0.6 mol B.等于1 mol
C.大于0.6 mol小于1 mol D.大于1 mol
查看答案和解析>>
科目: 来源: 题型:
A.碳酸钠(固体) B.水
C.硫酸钾溶液 D.硫酸铵(固体)
查看答案和解析>>
科目: 来源: 题型:
A.减小C或D的浓度 B.增大D的浓度
C.减小B的浓度 D.增大A或B的浓度
查看答案和解析>>
科目: 来源: 题型:
A.![]() (NH3)=0.010 mol·L-1·s-1 B.
(NH3)=0.010 mol·L-1·s-1 B.![]() (O2) =0.001 mol·L-1·s-1
(O2) =0.001 mol·L-1·s-1
C.![]() (NO)=0.001 mol·L-1·s-1 D.
(NO)=0.001 mol·L-1·s-1 D.![]() (H2O)=0.045 mol·L-1·s-1
(H2O)=0.045 mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
A.化学反应速率是指一定时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加
B.化学反应速率0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应来说,反应速率越大,反应现象就越明显
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
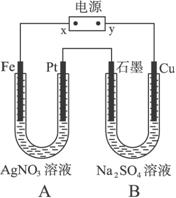
(1)电源上x为_________极。
(2)B池中阳极的电极反应式是_____________。
(3)标准状况时,如果在A中共收集到0.56 L气体,则A池中的pH为_____________。
查看答案和解析>>
科目: 来源: 题型:
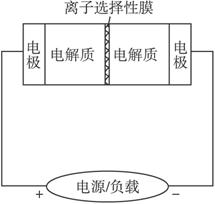
A.充电的过程中当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子
B.电池放电时,负极反应为:3NaBr-2e-====NaBr3+2Na+
C.充电过程中钠离子从右到左通过离子交换膜
D.放电过程中钠离子从右到左通过离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com