
科目: 来源: 题型:
Ⅰ. 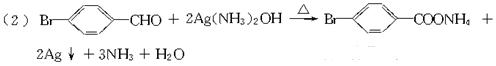 (R1、R2、R3代表烷烃基)
(R1、R2、R3代表烷烃基)
Ⅱ.烯醇式结构,即碳碳双键连接羟基(如CH2=CH—OH)不能稳定存在。
某有机物有如下转化关系:

(1)C7H5OBr中官能团名称为____________________________________。
(2)C7H5OBr与银氨溶液在加热时反应的化学方程式是(有机物写结构简式,下同):______________________________;实验现象是____________________________________。
(3)从C7H5OBr合成D通常要经过几步有机反应,其中最佳顺序是_________(填序号)。
a.水解、酸化、氧化 b.氧化、水解、酸化
c.水解、酸化、还原 d.氧化、水解、酯化
(4)若按“最佳顺序”进行,写出一定条件下B![]() C的化学反应方程式:________________。
C的化学反应方程式:________________。
(5)A有一种同分异构体,能与Na反应放出H2,则其结构简式为:____________________。
该有机物在一定条件下能发生加聚反应,其化学方程式为:________________________。
该反应所形成的高聚物吸水性强,原因可能是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)①完成并配平该氧化还原方程式:
________+________+________NH4Cl![]() ________+________+________+_______NH3
________+________+________+_______NH3
②发生还原反应的物质是_________,被氧化的元素是___________________________。
③若有

(2)普通锌—锰干电池是利用上述反应原理设计的,其结构如上图所示。回答下列问题:
①电池中电解质溶液为_________________________________________________。
②正极材料为______________;正极电极反应为______________________。
③放电时![]() 向________________(填“正极”或“负极”)移动。
向________________(填“正极”或“负极”)移动。
④普通锌—锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是__________________。
查看答案和解析>>
科目: 来源: 题型:
(1)X元素位于周期表中第____________族(用字母表示)。
(2)X、Y、Z三种元素形成的单质中,氧化性最弱的是____________________(填化学式)。
(3)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为_________________________________。
(4)a溶液的pH___________7(填“>”“<”或“=”),用离子方程式解释为__________________,若在a溶液中加入少量镁粉,可观察到的现象是_________________________________。
(5)取pH=0的W的最高价氧化物对应水化物的溶液100.0 mL于某容器中,加入
若设Cu、Ag的物质的量分别为x、y。欲求算x、y的值,可列出下列计算式:
Ⅰ.64x+108y=0.90,该计算式是依据_____________________________________关系列出的;
Ⅱ.2x+y=1 mol·L -1×
查看答案和解析>>
科目: 来源: 题型:

A.b曲线t2后,v正(B)=4v逆(D)
B.a曲线t1时,4v正(B)>v逆(D)
C.升高温度,可使曲线b变为曲线a
D.缩小反应容器的体积,可使曲线a变为曲线b
查看答案和解析>>
科目: 来源: 题型:
A
B.向Na2CO3溶液中加入少量NaHCO3固体,溶液pH减小
C.50 mL 1.0 mol·L-1的盐酸与60 mL 1.0 mol·L-1的盐酸分别跟50 mL 1.1 mol·L-1的NaOH溶液进行反应,中和热数值不相等
D.一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小
查看答案和解析>>
科目: 来源: 题型:
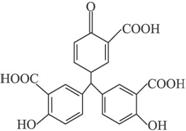
A.铝试剂分子中氢原子数目为16
B.1 mol 铝试剂最多消耗3 mol NaHCO3
C.铝试剂分子中所有碳原子可能在同一平面上
D.铝试剂能与FeCl3溶液发生显色反应
查看答案和解析>>
科目: 来源: 题型:
A.可用盐析的方法从油脂皂化反应后的混合物中分离出高级脂肪酸钠
B.实验室配制Fe(OH)3胶体是向沸水中滴入饱和FeCl3溶液,继续煮沸至溶液呈红褐色
C.从含有FeCl2、CuCl2的废液中回收Cu,可在废液中加盐酸调节其pH=1,用铜和石墨作电极进行电解。当阴极上有少量气泡产生时,表示铜已全部析出
D.检验纤维素的水解产物是在纤维素水解后的溶液中加入10 mL 1 mol·L-1的NaOH溶液,再加入5 mL 1 mol·L-1的CuSO4溶液,加热煮沸,观察现象
查看答案和解析>>
科目: 来源: 题型:
A.若Va=Vb,且NaOH与CH3COOH恰好完全反应,则a>2
B.若a=2,混合后溶液pH=7,则混合后V总>2Vb
C.若a=2,混合后溶液pH<7,则Va一定大于Vb
D.若Va=Vb,a=2,混合后溶液中微粒浓度的关系为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
A.甲酸钠溶液和盐酸混合:CH3COO-+H3O+![]() CH3COOH+H2O
CH3COOH+H2O
B.醋酸钠的水解反应:CH3COO-+H3O+![]() CH3COOH+H2O
CH3COOH+H2O
C.用石墨电极电解饱和MgCl2溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.向苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O![]() C6H5OH+
C6H5OH+![]()
查看答案和解析>>
科目: 来源: 题型:
A
B
C.标准状况下,
D.0.1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com