
科目: 来源: 题型:

①制取H2时,还缺少的固体试剂是_____________,(填名称)
反应的离子方程式:_____________;
②制取NO时,请你从上述试剂中为他选择比较合理的试剂是_____________;反应产生的气体需要用_____________法收集。
(Ⅱ)有一份由两种物质混合而成的白色混合物,分别取适量该混合物置于三支试管中进行实验:
①加热第一支试管中的白色混合物,试管口有水滴凝结;
②在第二支试管中逐滴加入4 mol·L-1的NaOH溶液至过量,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物;③在第三支试管中逐滴加入4 mol·L-1盐酸,同时不断振荡试管,有无色无味的气体产生,反应结束后得到无色透明溶液。
(1)符合以上实验现象的是_____________混合物(填选项);
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HSO3、MgCl2·6H2O D.NH4Cl、Ca(HCO3)2
(2)该混合物中的某一物质水溶液的pH<7,该物质是:_____________(填化学式);
(3)该混合物在实验②中产生白色不溶物的离子方程式:__________________________。
查看答案和解析>>
科目: 来源: 题型:
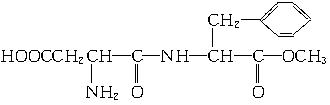
下列有关A的叙述中正确的是
A.A的分子式为:C14H13O5N2
B.A可以发生水解反应、中和反应、加成反应、消去反应
C.A物质完全水解的产物中,一定含有醇类
D.在一定条件下,1 mol A最多能与
查看答案和解析>>
科目: 来源: 题型:
A.化学反应速率变化时,化学平衡一定发生移动
B.只有在催化剂存在下,才会发生化学反应速率变化而化学平衡不移动的情况
C.可逆反应进行得越彻底,化学反应速率就越大
D.化学平衡发生移动时,化学反应速率一定变化
查看答案和解析>>
科目: 来源: 题型:
A.冰醋酸溶于水时,分子中羧基上的氢氧共价键部分发生断裂
B.原子及其离子的核外电子层数等于该元素所在的周期数
C.同一元素的各种同位素的物理性质、化学性质均相同
D.氯化钠熔化时离子键未被破坏
查看答案和解析>>
科目: 来源: 题型:
A.钠跟水的反应:2Na+2H+![]() 2Na++H2↑
2Na++H2↑
B.电解饱和食盐水:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.硫酸镁溶液跟氢氧化钡溶液反应:![]() +Ba2+
+Ba2+![]() BaSO4↓
BaSO4↓
D.酸性硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H++H2O2![]() Fe3++2H2O
Fe3++2H2O
查看答案和解析>>
科目: 来源: 题型:
A
B.1 mol液态CHCl3中原子总数等于NA
C.1 mol C5H12分子中所含单键数为16 NA
D.常温常压下,1 mol D216O中含中子数、质子数、电子数均为10 NA
查看答案和解析>>
科目: 来源: 题型:
原子种类 | N | S | O | Si |
原子半径(nm) | 0.075 | 0.102 | 0.074 | 0.117 |
根据以上数据,磷原子的半径可能是
A.0.100 nm B.0.110 nm C.0.080 nm D.0.070 nm
查看答案和解析>>
科目: 来源: 题型:
A.2Fe2++Cl2![]() 2Fe3++2Cl- B.2Fe3++SO2+2H2O
2Fe3++2Cl- B.2Fe3++SO2+2H2O![]() 2Fe2++
2Fe2++![]() +4H+
+4H+
C.H2O2+H2SO4![]() SO2↑+O2↑+2H2O D.I2+SO2+2H2O
SO2↑+O2↑+2H2O D.I2+SO2+2H2O![]() H2SO4+2HI
H2SO4+2HI
查看答案和解析>>
科目: 来源: 题型:
A.Zn粒 B.BaCl2溶液 C.KOH溶液 D.Ba(OH)2溶液
查看答案和解析>>
科目: 来源: 题型:
(2)
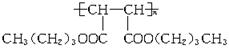
现仅以丙烯为有机原料,经过如下图所示的反应可以分别合成重要的化工原料F和K,以F和K为原料可合成一种链状高分子化合物M,其化学组成为(C12H20O4)n。
回答下列问题:
(1)反应①的反应类型是:____________。
(2)反应⑥、⑦中有一反应是与HCl加成,该反应是____________(填反应编号),设计这一步反应的目的是_______________________________________________________________。
(3)物质M的结构简式为__________________________________________________。
(4)反应⑧的化学方程式为_________________________________________________。
(5)D与新制Cu(OH)2反应的化学方程式为________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com