
科目: 来源: 题型:
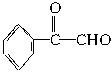
请回答下列问题:
(1)反应②使用的试剂X是_____________;
(2)物质C的结构简式是_____________,其中含有的含氧官能团有_____________;
(3)写出反应⑥的化学方程式:_______________________________________;
(4)乙同学通过分析,认为甲同学设计的步骤⑤存在明显缺陷。你认为,乙同学提出的缺陷是__________________________。
(5)甲、乙两同学经过查阅资料,自学了解了以下知识:
Ⅰ.R—CH2COOH+Br2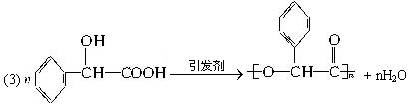
Ⅱ.CH3—CH=CH2![]() CH3—CH2—CH2Cl
CH3—CH2—CH2Cl
请根据以上新知识及学过的知识,设计反应流程图实现下列转化。

说明:合成反应流程图表示方法示例如下:
CH3CH2OH![]() CH3CHO……
CH3CHO……
查看答案和解析>>
科目: 来源: 题型:
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是_______________(填“氧化剂”或“还原剂”)。
②如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的化学方程式(不必配平):_________________________________。该反应中的氧化产物是________________。
(2)下图中,P为一个可以自由滑动的活塞。关闭K,分别向A、B两容器中各充入2 mol X和2 mol Y,在相同温度和有催化剂存在的条件下,两容器中各自发生如下反应:

2X(g)+Y(g)![]() 2Z(g)+2W(g)
2Z(g)+2W(g)
已知:起始时,VA=
①A、B两容器达到平衡的时间tA________________tB(填“大于”“小于”或“等于”);
②计算该温度下反应的化学平衡常数K=___________;
③当A、B分别达到平衡时,B容器中Y的转化率为____________,两容器中W的体积分数关系为A____________B(填“大于”“小于”或“等于”);
④打开K,一段时间后反应再次达到平衡,则此时B的体积为____________。
查看答案和解析>>
科目: 来源: 题型:
(1)元素C在周期表中的位置是________________;
(2)化合物M中含有的化学键类型有__________;
(3)写出化合物Y与Z之间反应的离子方程式:_______________________________;
(4)以铂作电极,以Y溶液作为电解质溶液,A、C元素的单质分别在两电极上发生原电池反应,则正极上的电极反应式为________________;若以该电池作为电源,用惰性电极电解
查看答案和解析>>
科目: 来源: 题型:

(1)写出反应Ⅰ的离子方程式_____________________。
(2)在D的水溶液中,各离子的浓度由大到小的顺序是_____________。
(3)取2 mL 0.1 mol·L-1的AgNO3溶液,向其中滴加2 mL 0.1 mol·L-1的C溶液,现象是_____________;然后继续向其中滴加0.1 mol·L-1的KI溶液,能否观察到明显现象?(若有,请写出实验现象和反应的离子方程式;若没有,请简要说明原因。)
查看答案和解析>>
科目: 来源: 题型:
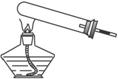
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①碳酸钠,②碳酸氢钠,③碳酸氢铵,④氯化铵,⑤熟石灰,⑥氢氧化钠
若A中制取气体时只用了一种药品,则该药品是____________(填物质序号),并在图中空白处将实验装置图补充完整(使用下列简易装置图,固定装置省略;使用尺、规作图)

(2)该装置补充完整后,仍然存在一定缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①________________________________。
②________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用是________________。
②写出C中发生反应的化学方程式:________________________________;
③若A处试剂足量,则装置D中可以观察到的实验现象有____________。
查看答案和解析>>
科目: 来源: 题型:
A.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
B.制备氢氧化铁胶体时,应向沸水中逐滴滴加1 mol·L-1的FeCl3溶液,并继续加热到液体呈透明的红褐色为止
C.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液滴在用蒸馏水湿润过的pH试纸上,并与标准比色卡比较
D.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂瓶中
E.除去蛋白质溶液中混有的NaCl,可以先加入AgNO3溶液,然后过滤
F.配制一定物质的量浓度的氢氧化钠溶液的过程,主要有称量、溶解、冷却、转移、洗涤和定容六步操作,其中,需要进行2次及以上的基本实验步骤有称量、转移和洗涤
查看答案和解析>>
科目: 来源: 题型:
①0.01 mol·L-1 CH3COOH;②0.01 mol·L-1 HCl;
③pH=12的氨水;④pH=12的NaOH溶液。
下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.将②③混合,若pH=7,则消耗溶液的体积:②=③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④;②>①
D.将①④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性
查看答案和解析>>
科目: 来源: 题型:
A.加入纯Cu将Fe2+还原
B.向溶液中加入(NH4)2S使Fe2+沉淀
C.直接加水加热使杂质离子水解除去
D.在溶液中通入Cl2,再加入CuO粉末调节pH为4—5
查看答案和解析>>
科目: 来源: 题型:
①滴有石蕊的CO2溶液 ②滴有石蕊的NH4Cl溶液 ③滴有石蕊的H2SO4溶液 ④滴有酚酞的氨水溶液 ⑤滴有酚酞的氢氧化钠溶液 ⑥滴有酚酞的饱和氢氧化钙溶液 ⑦滴有酚酞的Na2CO3溶液 ⑧溶有SO2的品红溶液
A.①④⑥ B.④⑥⑧ C.③⑤⑦⑧ D.②④⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com