
科目: 来源: 题型:
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 ②用NaOH溶液除去苯中的少量苯酚 ③用饱和NaHCO3溶液除去CO2中的少量SO2 ④用加热的方法提取NH4Cl固体中混有的少量碘 ⑤用醋酸和澄清石灰水验证蛋壳中含有碳酸盐 ⑥用米汤检验食用加碘盐中含碘 ⑦用碘酒验证汽油中含有不饱和烃
A.①②④⑤⑦ B.②③⑤⑦ C.②③④⑤ D.①②③④⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.在共价化合物分子内,一定不存在离子键
D.由不同元素组成的多原子分子里,一定只存在极性键
查看答案和解析>>
科目: 来源: 题型:
A.大力开发氢能源 B.充分利用太阳能
C.不使用含碳能源 D.提高能源利用率
查看答案和解析>>
科目: 来源: 题型:
1.[化学—有机化学基础]
下列框图表示A、B、C、D、E、F、G、H、I各物质间的转化关系,已知有机物H分子中含有5个碳原子。有机物I是一种高分子材料。

已知R—CN![]() R—COOH
R—COOH
请回答下列问题:
(1)物质D和I的结构简式为:
D___________________,
I__________________。
(2)指出反应类型:反应④属___________,⑥属___________。
(3)写出下列反应的化学方程式:
反应②_______________________________________________________________。
反应⑦_______________________________________________________________。
(4)写出与H具有相同官能团且只含有一个甲基的同分异构体的结构简式(除H外,请写出任意两种)________________________,________________________。
2.[化学—物质结构与性质]
今有位于元素周期表短周期中的X、Y、Z三种元素。已知:
①三者原子序数之和为25;
②元素Y的原子价电子排布为ns2npn+2;
③X和Y在不同条件下可形成X2Y和X2Y2两种固态化合物,Y和Z在不同条件下可形成ZY和ZY2两种气态化合物;
④元素Z的硫化物与元素Z的氯化物,常温下均为液态,且二者的相对分子质量之比为38∶77。
据此填写下列空白:
(1)写出元素符号:
X____________;Y____________;Z____________。
(2)X2Y2属于___________晶体,构成晶体的微粒是________________(填微粒符号)。
(3)Z的硫化物的分子空间构型是_________________________,ZY2形成的晶体属于______________________晶体,根据原子轨道重叠方式的不同,Z的氯化物分子中含有的共价键种类及数目是__________________________。
查看答案和解析>>
科目: 来源: 题型:
请回答下列问题:
(1)HgS与O2的反应中,氧化剂是____________,每生成1 mol Hg转移电子的物质的量为____________ mol。
(2)电解某汞的硝酸盐溶液,当阴极消耗a mol金属阳离子时,可获得
(3)随着冶炼、电镀等工业生产的不断发展,所需汞及其化合物的用量也日趋增多,随之排放出来的含汞的废水也愈加严重,现已成为世界上危害较大的工业废水之一。以下处理含汞(Hg2+)废水的方法中最简单实用的是____________(填序号)。
A.向含Hg2+的废水中加入Na2S等可溶性硫化物
B.加入金属还原剂
C.电解法
查看答案和解析>>
科目: 来源: 题型:
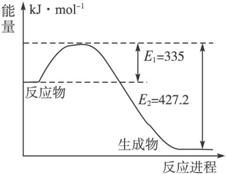
(1)上图是N2和H2反应生成2 mol NH3过程中能量变化示意图,请计算每生成1 mol NH3放出热量为____________。
(2)在一定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)![]() 2NH3(g),其化学平衡常数K与温度t的关系如下表:
2NH3(g),其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | … |
K/(mol·L-1)-2 | 4.1×106 | K1 | K2 | … |
请完成下列问题:
①试比较K1、K2的大小,K1________K2(填写“>”“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据的是__________(填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.2v(N2)正=v(H2)逆
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式________________________。
②盐酸肼水溶液中离子浓度的关系表示正确的是___________(填序号)。
A.c(Cl-)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O]+)>c(OH-)>c(H+)
C![]() )+c ([N2H5·H2O]+)+c(H+)=c(Cl-)+c(OH-)
)+c ([N2H5·H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(![]() )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在元素周期表中位置________。
(2)写出C、H物质的化学式:C______________________,H_____________________。
(3)写出反应①⑦的化学方程式:
反应①:____________________________________________________________。
反应⑦:_____________________________________________________________。
(4)反应⑥过程中的现象是____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解

①配制浓度均为1 mol·L-1的盐酸和醋酸溶液;
②在广口瓶乙中装水,按图示连接好装置,检查装置的气密性;
③量取10.00 mL 1 mol·L-1的盐酸和醋酸溶液分别加入两套装置的锥形瓶中;
④称取两份质量均为a g的镁条(除去表面氧化膜、表面积相同),并固定于塑料杆末端;
⑤同时将塑料杆向下移动,使镁条浸入酸中至反应完全;
⑥反应结束后待温度恢复到室温,读出量筒中水的体积为V mL。
请根据上述步骤回答下列问题:
(1)用文字表述步骤②中检查该装置气密性的方法:_____________________。
(2)量取10.00 mL1mol·L-1盐酸和醋酸溶液分别注入锥形瓶中时,所用的仪器是_________(填下列各项序号字母)。
A.50 mL量筒 B.10 mL量筒
C.25 mL酸式滴定管 D.25 mL碱式滴定管
(3)步骤④中,理论上称取的镁条质量不能少于_________ g。
(4)步骤⑤中需记录的数据是_______;实验过程中观察到的主要现象是______________。
(5)步骤⑥中,读取量筒中水的体积时若俯视读数,对计算该条件下的气体摩尔体积影响为_________(填“偏大”“偏小”或“无法确定”)。
(6)为保证实验顺利进行,仪器丙应选用的规格是_________(填序号字母)。
A.100 mL B.200 mL C.500 mL
(7)若水蒸气的挥发影响忽略不计,在该温度和压强下,气体摩尔体积为______ L·mol-1。
查看答案和解析>>
科目: 来源: 题型:
①在加油站内拨打手机
②在煤矿巷道内用明火照明
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约药品,锌与稀硫酸一开始反应,就做氢气点燃实验
⑤稀释浓硫酸时,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌
(2)下图为常见仪器的部分结构(有的仪器被放大):

A图中液面所示溶液的体积为_________ mL,C图中液面所示溶液的体积为_________ mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是_________(填仪器序号字母)。
(3)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的瓷质仪器的名称为________________________。
②该同学将所得精盐配成溶液,用于另一实验。实验中需要用100 mL 1 mol·L-1的NaCl溶液,配制过程中需用托盘天平称取的精盐质量为_________ g,用于定容的玻璃仪器的规格和名称____________。
查看答案和解析>>
科目: 来源: 题型:
A.等于0.3 mol B.等于0.15 mol
C.小于0.15 mol D.大于0.15 mol,小于0.3 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com