
科目: 来源: 题型:
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极
查看答案和解析>>
科目: 来源: 题型:
A.C(s)+H2O(g)![]() CO(g)+H2(g);ΔH>0
CO(g)+H2(g);ΔH>0
B.Ba(OH)2·8H2O+2NH4Cl(s)![]() BaCl2(aq)+2NH3·H2O(l)+8H2O(l);ΔH>0
BaCl2(aq)+2NH3·H2O(l)+8H2O(l);ΔH>0
C.CaC2(s)+2H2O(l)![]() Ca(OH)2(s)+C2H2(g);ΔH<0
Ca(OH)2(s)+C2H2(g);ΔH<0
D.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH<0
CO2(g)+2H2O(l);ΔH<0
查看答案和解析>>
科目: 来源: 题型:
A.4FeS2(s)+11O2(g)![]() 2Fe2O3(s)+8SO2(g);ΔH=+853.7 kJ·mol-1
2Fe2O3(s)+8SO2(g);ΔH=+853.7 kJ·mol-1
B.FeS2(s)+![]() O2(g)
O2(g)![]()
![]() Fe2O3(s)+2SO2(g);ΔH=-853.7 kJ·mol-1
Fe2O3(s)+2SO2(g);ΔH=-853.7 kJ·mol-1
C.4FeS2(s)+11O2(g)![]() 2Fe2O3(s)+8SO2(g);ΔH=+3 414.8 kJ·mol-1
2Fe2O3(s)+8SO2(g);ΔH=+3 414.8 kJ·mol-1
D.FeS2(s)+![]() O2(g)
O2(g)![]()
![]() Fe2O3(s)+2SO2(g);ΔH=-3 414.8 kJ·mol-1
Fe2O3(s)+2SO2(g);ΔH=-3 414.8 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.9 g D2O中含有的电子数为5NA
B.气体摩尔体积是指在标准状况下1 mol任何气体所占的体积
C.1 mol CH4分子中共价键总数为4NA
D.7.1 g Cl2与足量NaOH溶液反应转移的电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
A.“暖冰”也是水分子间通过氢键结合而成的固体
B.水凝固形成20 ℃时的“暖冰”所发生的变化是化学变化
C.形成20 ℃时的“暖冰”的变化是物理变化
D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
查看答案和解析>>
科目: 来源: 题型:
A.氧元素的一种同位素 B.臭氧的同素异形体
C.一种新的氧化物 D.可能是极性键构成的极性分子
查看答案和解析>>
科目: 来源: 题型:
(1)试分析,欲求标准状况下生成的CO2气体的体积时,还需要什么数据___________(用a表示,并注明单位)。
(2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表):
| 所需数据取值范围 | 生成CO2气体的体积 |
盐酸不足量时 |
|
|
盐酸足量时 |
|
|
(3)若NaHCO3和KHCO3的物质的量不相等,则4.60 g的混合物与足量盐酸完全反应时,在标准状况下生成的CO2气体的体积大于____________L,小于____________L。
查看答案和解析>>
科目: 来源: 题型:
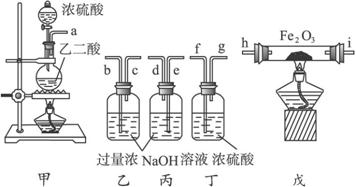
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a,b……表示)a接b,c接___________,___________接___________,___________接___________。
(2)装置丙的作用是___________________________________。
(3)怎样除去尾气中的CO气体?_________________________________。
(4)实验前氧化铁矿粉末为x g,经充分反应实验后测得乙、丙质量分别增加y g和z g,则该矿石中氧化铁的质量分数为___________。
查看答案和解析>>
科目: 来源: 题型:
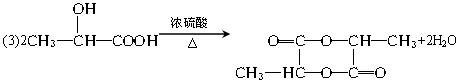
 ,
,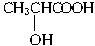 链烃;A能发生如下图所示的一系列变化:
链烃;A能发生如下图所示的一系列变化:
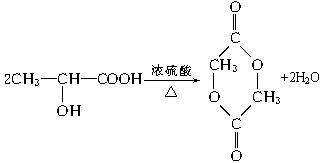
在上述转化中,已知:C的分子式为C3H8O2,2个E分子间可脱去水分子缩合生成六元环状化合物C6H8O4,试填写下列空白:
(1)写出链烃A的名称:_______________。
(2)在反应①—⑦中属于取代反应的是_______________________。
(3)写出2分子E脱去水分子缩合生成六元环C6H8O4化合物的化学方程式:_________。
(4)写出反应⑦的化学方程式:______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com