
科目: 来源: 题型:
A.两种液体都是红褐色
B.分散质粒子都能通过半透膜
C.分散质粒子大小都在1 nm—100 nm之间
D.加热、蒸干、灼烧后,得到相同的固体
查看答案和解析>>
科目: 来源: 题型:
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
A.干冰升华时,分子内共价键不会发生断裂
B.分子晶体中的每个分子内一定含有共价键
C.原子晶体中的相邻原子间只存在非极性共价键
D.仅由非金属元素形成的化合物不可能是离子化合物
查看答案和解析>>
科目: 来源: 题型:
A.Na2CO3、NaHCO3、NaCl、NH4Cl B.Na2CO3、NaHCO3、NH4Cl、NaCl
C.(NH4)2SO4、NH4Cl、NaNO3、Na2S D.NH4Cl、(NH4)2SO4、Na2S、NaNO3
查看答案和解析>>
科目: 来源: 题型:
A.绿色食品是不含任何化学物质的食品
B.推广使用太阳能、风能、海洋能、氢能,不利于缓解温室效应
C.在含硫的燃料中加入适量生石灰,可以减少二氧化硫的排放量
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
查看答案和解析>>
科目: 来源: 题型:
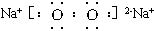
(1)A的化学式为____________________。
(2)N的电子式为____________________,所含化学键为____________________。
(3)A→C的离子方程式为________________________________。
(4)C→D的化学方程式为________________________________。
(5)已知标准状况下有
查看答案和解析>>
科目: 来源: 题型:
(1)“502胶”是一种快干胶,其主要成分是α氰基丙烯酸乙酯,其结构简式为:
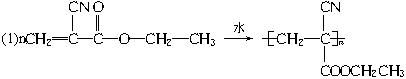 ,它在空气中微量水催化下发生加聚反应,迅速固化而将被黏物粘牢。请写出“502胶”发生黏合过程的化学方程式:________________________。
,它在空气中微量水催化下发生加聚反应,迅速固化而将被黏物粘牢。请写出“502胶”发生黏合过程的化学方程式:________________________。
(2)厌氧胶也是一种黏合剂,其结构简式为:
![]() ,它在空气中稳定,但在隔绝空气(缺氧)时分子中双健断开发生聚合而固化。工业上用丙烯酸(CH2=CH—COOH)和某种物质在一定条件下反应可制得这种黏合剂。请写出这一制取过程的化学方程式:__________。
,它在空气中稳定,但在隔绝空气(缺氧)时分子中双健断开发生聚合而固化。工业上用丙烯酸(CH2=CH—COOH)和某种物质在一定条件下反应可制得这种黏合剂。请写出这一制取过程的化学方程式:__________。
(3)乳白胶是一种常见黏合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),其中同时含有“—CHO”和“—CH=CH—”结构的同分异构体有多种,如:
“CH3—CH=CH—O—CHO”和“CH2=CH—CH2—O—CHO”,请再写出三种能稳定存在的同分异构体的结构简式(已知含有![]() 的结构不能稳定存在___________________,______________________,______________________________。
的结构不能稳定存在___________________,______________________,______________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)写出下列元素的元素符号:B________,D________;写出E的两种常见同素异形体的名称________;C、E的氢化物的沸点高低关系是________(用分子式和“>”表示)。
(2)X是C的最高价氧化物的水化物,它是重要的化学试剂,其浓溶液需避光保存,这是因为(用化学方程式表示)____________________________________。
(3)Y是C的最高价氧化物的水化物和其氢化物反应生成的化合物,常温时,pH=a的X、Y两种溶液中由水电离出来的H+浓度之比为__________________。
(4)X与A、B组成的某化合物在一定条件下反应制得一种常见的烈性炸药,其反应的化学方程式为____________________________________。
(5)由上述元素组成的某化合物其化学式为B
查看答案和解析>>
科目: 来源: 题型:

A中放有
试回答下列问题:
(1)请写出在蒸发皿中制得莫尔盐的化学方程式:_________________________________。
(2)滴加稀硫酸时,发现其反应速率比同浓度硫酸与纯铁粉反应快,其原因是___________
_____________________________________。
(3)取
①配平下列反应式:
______Fe2++______![]() +______H+——______Mn2++______Fe3++______H2O
+______H+——______Mn2++______Fe3++______H2O
②用________(酸式或碱式)滴定管盛装高锰酸钾溶液。
③高锰酸钾溶液的物质的量浓度是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com