
科目: 来源: 题型:
火力发电是通过化石燃料燃烧,使化石燃料中化学能转化为电能,其能量转化方式正确
的是 ( )
A.化学能 → 电能 B.化学能 → 机械能 →电能
C.化学能 → 热能 →电能 D.化学能 → 热能 → 机械能 →电能
查看答案和解析>>
科目: 来源: 题型:
三峡工程水电站装机总容量是1820万千瓦,这将给中国电网带来历史性变革,有利于全国电力联网和西电东输工程。目前在我国发电总量中的比例最大的是 ( )
A.水电(水力发电) B.火电(火力发电)
C.核电(核能发电) D.风电(风力发电)
查看答案和解析>>
科目: 来源: 题型:
下列关于电能的特点叙述中错误的是 ( )
A.电能较其它能源使用方便
B.电能在现代社会中的使用最为广泛
C.电能使用导致的污染小
D.电能是化学能与各种能量转化中利用率最高的
查看答案和解析>>
科目: 来源: 题型:
抗流感药物达菲(Tamiflu)是以莽草酸(A)为原料,经过十步反应合成制得。莽草酸可以从我国常用的烹调香料“八角”中提取。达菲及A(莽草酸)的结构简式如下:
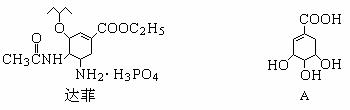
已知:![]()
化合物A、B、C、D、E之间存在下图所示的转化关系。已知B遇FeCl3显紫色,且环上的一溴代物有两种。(提示: ![]() 可表示为:
可表示为:![]() )
)
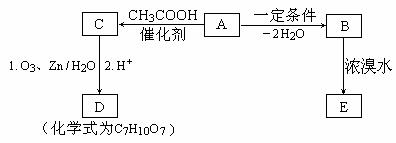
请回答下列问题:
(1)写出化合物A中所含无氧官能团的名称: ;
(2)写出A→B的反应类型________________;
(3)写出B→E的化学方程式: ;
(4)写出D的结构简式: ;
(5)设计A生成C的目的 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+、Cu2+等杂质)生产医药级二水合氯化钙(CaCl2?2H2O的质量分数为97.0%~103.0%)的主要流程如下:
![]()
![]()
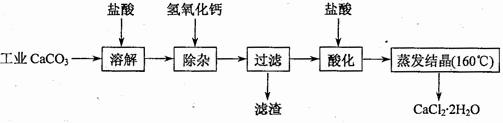
![]() (1)除杂操作是加入氢氧化钙,调节溶液的pH,以除去溶液中的少量Al3+、Fe3+、Cu2+。
(1)除杂操作是加入氢氧化钙,调节溶液的pH,以除去溶液中的少量Al3+、Fe3+、Cu2+。
①已知Cu(OH)2的KSP=2×l0-20 (mol/L)3。要使0. 2mol?L-1CuCl2溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一,此时Al3+、Fe3+已沉淀完全),则应向溶液里加入强碱溶液至溶液的pH为______。
②检验Fe(OH)3已经沉淀完全的实验操作是 ;
③如果将氢氧化钙改为纯净的碳酸钙,请用离子方程式表达除去溶液中Fe3+的过程:
。
![]() (2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其主要目的是: 。
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其主要目的是: 。
![]() (3)测定样品中Cl-含量的方法是:a.称取0.75g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
(3)测定样品中Cl-含量的方法是:a.称取0.75g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
![]() ①上述测定过程中需要溶液润洗的仪器有 。
①上述测定过程中需要溶液润洗的仪器有 。
![]() ②量取25.00mL待测溶液于锥形瓶中时,如果开始滴定管的液面读数为5.10mL,左手控制滴定管的活塞,使待测溶液流入锥形瓶中,眼睛注视着 ,直到 ,迅速关闭活塞。
②量取25.00mL待测溶液于锥形瓶中时,如果开始滴定管的液面读数为5.10mL,左手控制滴定管的活塞,使待测溶液流入锥形瓶中,眼睛注视着 ,直到 ,迅速关闭活塞。
③计算上述所得样品中CaCl2?2H2O的质量分数为 。
![]() ④若用上述办法测定的样品中CaCl2?2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 ; 。
④若用上述办法测定的样品中CaCl2?2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 ; 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2。
2CO2+N2。
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)= 。
(3)在该温度下,反应的平衡常数K= 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
①请在上表空格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。
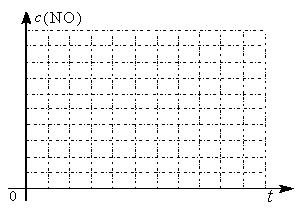
![]()
查看答案和解析>>
科目: 来源: 题型:
2009年10月山东主办的十一届全运会火炬“如意”的燃料丙烷是清洁能源。人们已经研究出以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐,电池总反应方程式为:C3H8 +5O2 = 3CO2+ 4H2O。
(1)已知: 2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) ∆H1
C(s) + O2(g) = CO2(g) ∆H2
2C(s) + O2(g) = 2CO(g) ∆H3
则C3H8(g) +5O2((g) = 3CO2(g) + 4H2O(l) ∆H= (用∆H1 、∆H2 、∆H3表示)
(2)写出该电池正极的电极反应式: ,电池工作时CO32-移向 ;用该电池电解1000 mL 1mol/L的AgNO3溶液,此电解池的反应方程式为 ;当电池消耗0.005 mol C3H8时,被电解溶液的pH为 (溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com