
科目: 来源: 题型:
下列说法正确的是
A.pH=5的![]() 溶液或醋酸中,由水电离出的
溶液或醋酸中,由水电离出的![]() 均为10
均为10![]() mol/L
mol/L
B.pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7
C.在c(H![]() ):c(OH
):c(OH![]() )=1:10
)=1:10![]() 的溶液中,Na
的溶液中,Na![]() 、I
、I![]() 、
、![]() 、
、![]() 能大量共存
能大量共存
D.0.1 mol/L![]() 溶液和0. 1 mol/L
溶液和0. 1 mol/L![]() 溶液等体积混合,溶液中
溶液等体积混合,溶液中
![]()
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.将铁粉加入![]() 、
、![]() 混合溶液中,充分反应后剩余的固体中必有铁
混合溶液中,充分反应后剩余的固体中必有铁
B.将![]() 和
和![]() 混合气体分别通入
混合气体分别通入![]() 溶液、
溶液、![]() 溶液中,最终都有沉淀生成
溶液中,最终都有沉淀生成
C.检验某酸性溶液中![]() 和
和![]() ,选用试剂及顺序是过量
,选用试剂及顺序是过量![]() 溶液、
溶液、![]() 溶液
溶液
D.用加热分解的方法可将![]() 固体和Ca(OH)2固体的混合物分离
固体和Ca(OH)2固体的混合物分离
查看答案和解析>>
科目: 来源: 题型:
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,![]() 和
和![]() 离子的电子数之差为8。下列说法不正确的是
离子的电子数之差为8。下列说法不正确的是
A.与W相邻的同主族元素可制成重要的半导体材料
B.元素原子半径从大到小的顺序是X、Y、Z
C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构
D.W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是![]()
查看答案和解析>>
科目: 来源: 题型:
下列实验操作不能达到其对应目的的是
| 编号 | 实验操作 | 目的 |
| A | 取 (水的密度近似看作1g/ | 配置4% |
| B | 滴定实验中,用待测液润洗锥形瓶 | 避免造成误差使滴定结果偏低 |
| C | 向 | 证明升高温度能促进 |
| D | 向盛有铜片的试管中加入浓硫酸,加热 | 证明浓硫酸具有强氧化性 |
查看答案和解析>>
科目: 来源: 题型:
反应![]() 的能量变化如右图所示。下列说法正确的是
的能量变化如右图所示。下列说法正确的是
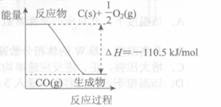 A.12 g C(s)与一定量
A.12 g C(s)与一定量![]() (g)反应生成14 g CO(g)
(g)反应生成14 g CO(g)
放出的热量为110.5 kJ
B.2 mol C(s)与足量![]() (g)反应生成
(g)反应生成![]() (g),
(g),
放出的热量大于221 kJ
C.该反应的热化学方程式是
![]()
![]()
D.该反应的反应热等于CO分子中化学键形成
时所释放的总能量与![]() 分子中化学键断裂时所吸收的总能量的差
分子中化学键断裂时所吸收的总能量的差
查看答案和解析>>
科目: 来源: 题型:
下列事实不能用金属活动性解释的是
A.生活中可用铝制的水壶烧水
B.镀锌铁制品破损后,镀层仍能保护铁制品
C.工业上常用热还原法冶炼铁,用电解法冶炼钠
D.电解法精炼铜时,其含有的Ag、Au杂质沉积在电解槽的底部
查看答案和解析>>
科目: 来源: 题型:
已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质: 如:![]()
A―F是六种有机化合物,它们之间的关系如下图,请根据要求回答:
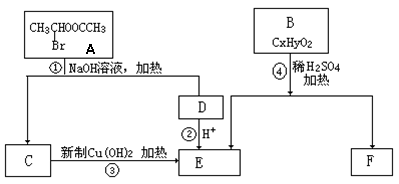 |
(1)在一定条件下,经反应①后,生成C和D,C的分子式为 ,反应①的类型为 。
(2)反应③的化学方程式为 .
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有 种结构,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目: 来源: 题型:
以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵[(NH4)2S2O8]和氧化铁红颜料, 原料的综合利用率较高。其主要流程如下:
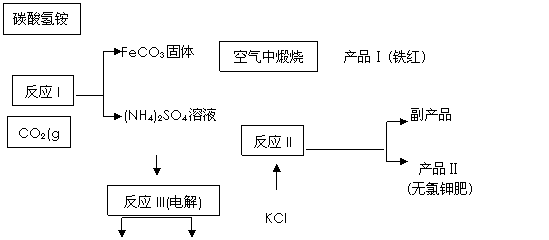 | |||
| |||
|
(1)①反应I前需在FeSO4 溶液中加入 ,以除去溶液中的Fe3+;
②反应I需控制反应温度低于35℃,其目的是 。
(2) ①反应II所得的副产品是 ;试写出该副产品的一种用途为 。
②检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,
。
(3)煅烧FeCO3生成产品I的化学反应方程式为________________________。实验室进行煅烧操作所需仪器除了酒精灯、泥三角、三脚架、玻璃棒外,还有 。
(4)反应III常被用于电解生产(NH4)2S2O8 (过二硫酸铵)。电解时均用惰性电极,阳极 发生的电极反应可表示为: 。
查看答案和解析>>
科目: 来源: 题型:
为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
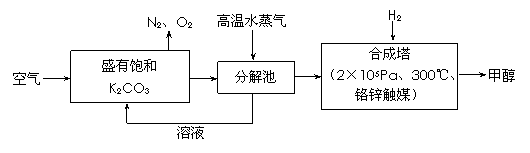
(1)在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947 kJ的热量,试写出合成塔中发生反应的热化学方程式是 。
(2)以甲醇为燃料制作新型燃料电池,电池的正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是:
CH3OH + H2O - 6e- ==== CO2 + 6H+
则正极发生的反应是 ;放电时,H+移向电池的 (填“正”或“负”)极。
(3)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5 mol?L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3-+H+ 的平衡常数K = 。(已知:10-5.6=2.5×10-6)
HCO3-+H+ 的平衡常数K = 。(已知:10-5.6=2.5×10-6)
(4)常温下,0.1 mol?L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-) (填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。小李应该选用的试剂是___________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验可能用到的仪器如下图所示:
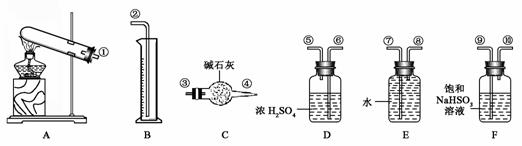 |
【提出猜想】
Ⅰ.所得气体的成分可能只含 一种;
Ⅱ.所得气体的成分可能含有 二种;
Ⅲ.所得气体的成分可能含有 三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。请回答下列问题:
(1) 请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
__ (填序号)
(2) 若实验结束,B中量筒没有收集到水,则证明猜想 正确。
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由。答:
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4 的质量(g) | 装置C增加 的质量(g) | 量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:_____________ ;
二组:_ 。
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是________和_______(填代号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com