
科目: 来源: 题型:
下述实验中不能达到预期实验目的的是( )
| 编号 | 实验内容 | 实验目的 |
| A | C2H5Cl和NaOH溶液混合后振荡再加入AgNO3溶液 | 检验C2H5Cl中的Cl元素 |
| B | 向沸腾的水中滴加FeCl3饱和溶液,继续煮沸至溶液呈红褐色为止 | 制备Fe(OH)3胶体 |
| C | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| D | 室温下,用pH计测定浓度各为0.1mol/LNa2CO3溶液和CH3COONa溶液的pH | 比较H2CO3和CH3COOH的酸性强弱 |
![]()
查看答案和解析>>
科目: 来源: 题型:
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则下列说法正确的是 ( )
A.反应过程中能得到6.72L的气体 B.最终得到的溶液中c(Na+)= c(Cl-) + c(OH-)
C.最终得到15.6g的沉淀 D.最终得到的溶液中c(NaCl)=1.5mol/L
![]()
查看答案和解析>>
科目: 来源: 题型:
室温下,下列混合溶液中,各离子浓度的关系正确的是( )
A.pH=12的氨水溶液与pH=2的盐酸溶液等体积混合c(NH4+)﹥c(Cl—)﹥c(OH—)﹥c(H+)
B.浓度均为0.1mol/L的硫酸氢铵溶液与氢氧化钠溶液等体积混合
c(Na+)﹥c(SO42—)﹥c(NH4+)﹥c(H+)﹥c(OH—)
C、浓度为0.1mol/L的碳酸钠溶液c(Na+)+ c(H+)=2c(CO32—)+c(OH—)www.ks%5……u.cD、浓度为0.1mol/L的醋酸钠溶液c(OH—)= c(H+)+ c(CH3COOH)+ c(CH3COO-)
![]()
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是( )
①亚硫酸钠溶液中加入硝酸:SO32-+2H+=H2O+SO2↑
②铜片跟浓硝酸反应:Cu+2NO3-+4H+ =Cu2++2NO2↑+2H2O
③向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3?H2O+H2O
④0.1molFeBr2中通入0.1molCl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2 +6Cl-
⑤硫化钠的水解:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
⑥向苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO 3-
A.①②③ B.②③⑥ C.③④⑥ D.④⑤⑥
![]()
查看答案和解析>>
科目: 来源: 题型:
有研究发现,奥司他韦可以有效治疗H1N1 流感,奥司他韦分子式为C16H28N2O4·H3PO4,分子结构如图。下列有关奥司他韦的说法中正确的是( )
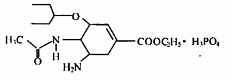
A.只含极性键,易溶于水,其水溶液有丁达尔效应
B.分子中含有酯基、氨基、苯环等官能团
C.1mol 该物质最多能与3mol ![]() 反应
反应
D.可以发生加成、取代、氧化反应
![]()
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是(NA表示阿伏加德罗常数) ( )
A.标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数约为1.5NA个
B.常温常压下,1mol氦气含有的核外电子数为4NA
C.1L1 mol•L-1的氯化铁溶液中铁离子的数目为NA
D.标准状况下,以任意比例混合的甲烷和丙烷混合气体22.4L,所含的气体分子数约为NA个
![]()
查看答案和解析>>
科目: 来源: 题型:
化学与生产、生活、科技等密切相关。下列说法正确的是( )
A.把世博会期间产生的垃圾焚烧或深埋处理
B.国务院要求坚决控制钢铁、水泥、焦炭等行业产能总量是落实“低碳经济”的具体举措
C.苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理
D.“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃
![]()
查看答案和解析>>
科目: 来源: 题型:
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的电子排布式为 ▲ 。
(2)卤素互化物如BrI、ICl等与卤素单质结构相似、性质相近。Cl2、BrI、ICl沸点由高到低的顺序为 ▲ 。
(3)多卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为 ▲ 。
(4)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为 ▲ 。
(5)气态氟化氢中存在二聚分子(HF)2,这是由于 ▲ 。
(6)①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]的酸性由强到弱的顺序为 ▲ (填序号)。
查看答案和解析>>
科目: 来源: 题型:
合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨,制得的氨通过催化氧化可生产硝酸。
在一定条件下,若N2和H2以体积比1:3的比例充入一体积不变的密闭容器中反应,达到平衡状态时,测得混合气体中氨的体积分数为20.0%,则:
(1)合成氨反应达到平衡的标志 ▲ 。
A.容器内气体压强保持不变
B.容器内各物质的浓度不随时间变化
C.当υ(H2,正)=0.3mol·L-1·min-1,υ(NH3,逆)=0.2mol·L-1·min-1时
D.1个N≡N键断裂的同时,有3个H-H键形成
(2)达到平衡时,N2和H2的转化率分别为 ▲ 。
(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
▲ 。
(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下:
![]()
其中反应②为:4NO+3O2+2H2O![]() 4HNO3,原料气为氨气和空气的混合物。
4HNO3,原料气为氨气和空气的混合物。
若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
某芳香烃的分子式为C12H14,其苯环上的一氯代物只有一种,A能发生如下图所示的转化,并最终制得合成纤维J和合成橡胶K。(某些反应条件已略去)
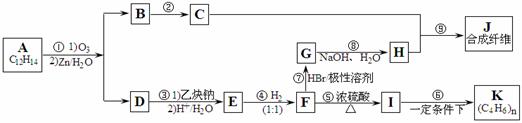
已知:

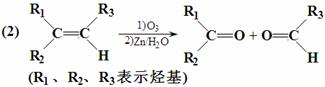
![]()
Ⅰ.请回答下列问题:
(1) A的结构简式 ▲ 。
(2)上述转化发生的反应中,属于消去反应的是 ▲ 。
(3)反应⑨的化学方程式是 ▲ 。
(4)请写出两种符合下列条件的B的同分异构体的结构简式:
①能与FeCl3溶液反应显色;②能与溴的CCl4溶液发生加成反应;③苯环上有三个取代基。
▲ 、 ▲ 。
Ⅱ.3-戊醇可作香料。以甲醛和乙炔钠为原料,其他试剂自选,完成其合成路线。
![]() ▲ 。
▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com