
科目: 来源: 题型:
已知A是卤代烃,C是高分子化合物,H是一种环状酯。转化关系如下图所示。
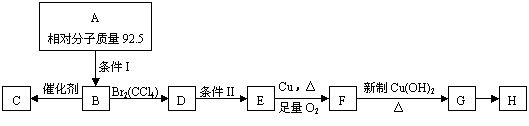
回答下列问题:
(1)A的分子式 ;D→E的反应类型: ,条件I是 。
(2)写出E、H的结构简式:E: ,H: 。
(3)写出下列反应的化学方程式:
B→C: ;
F→G: 。
(4)满足下列条件的G的同分异构体有 种。
①属于酯类;②能发生银镜反应;③能与金属钠反应放出气体。
查看答案和解析>>
科目: 来源: 题型:
已知A是含有两种元素的有机溶剂,分子结构与C相似。F是一种黄色固体,H是一种白色粉末,B、F、L、O、P是中学常见单质,J的相对分子质量比D大16。反应①是侯氏制碱法的重要反应。在一定条件下有如下反应关系:
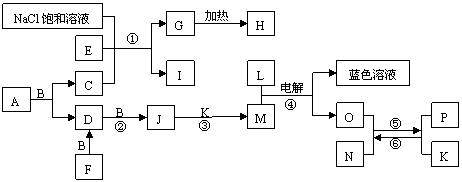
(1)组成单质P的元素在周期表中的位置为 。A的电子式为 ,G的俗名为: 。
(2)N与M的稀溶液反应的离子方程式为 。
(3)反应①的化学方程式为 。
(4)反应④中阳极的电极反应式为 。
(5)当反应⑤在高温下生成1.5molP时转移的电子数为 。
查看答案和解析>>
科目: 来源: 题型:
化学课外活动小组设计了如图所示的一套气体发生、收集和尾气处理装置,以探究该装置的多功能性。

(1)甲认为装置I可作为实验室快速制氧气的发生器,则装置I的a仪器中可加入 。b仪器中加入 。装置II从 管口进气可作为O2的收集装置。
(2)乙认为装置I可以支取乙炔,则装置I的a仪器中可加入 (写名称)。b仪器中加入 (写名称)。写出实验室制取乙炔的化学方程式:
。
(3)丁认为装置I和装置III,可验证Cl2的氧化性比Br2强,进行此项实验时在装置I中a仪器中加入 (写名称)。b仪器中加入 。装置III中应加入适量的 (写化学式),根据装置III中观察到 的现象即可得出Cl2的氧化性比Br2强的结论。
(4)丙认为利用装置II可收集NO,试简述操作方法:
。
查看答案和解析>>
科目: 来源: 题型:
CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
I、将CO2转化成有机物可有效实现碳循环
(1)CO2转化成有机物的例子很多,如:

以上反应中,原子利用率最高的是 。
(2)科学家最近成功开发出一种能将CO2转化为液体燃料的转基因蓝藻。这种蓝藻能通过光合作用消耗CO2并产生异丁醇[(CH3)2CHCH2OH],其名称是 (系统命名法)。实验测得37g异丁醇完全燃烧放出1333.8kJ热量,用热化学方程式来表示异丁醇的燃烧热: 。
II、开发低碳能源是未来的发展趋势
锂——空气电池能够提供相当于普通锂电池10倍的能量,因此它是最有前途的电池技术。下图是锂——空气电池放电和充电时的工作示意图。

(3)图I中电极a是 极。
(4)用锂——空气电池电解100mL0.5mol/LCuSO4溶液,当电池中消耗1.4gLi时,在阴极会析出 g铜
(5)电池中间的固体电解质(含阳离子交换膜)还能阻止H2O、N2、O2等物质的通过,防止Li和这些物质反应。Li和水在常温下发生反应的化学方程式为
。
(6)当给图II中的锂空气电池充电时,d极应接电源的 极,该电极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
 将由FeSO4、Ba(OH)2、AlCl3三种固体组成的混合物溶于足量的水中,用玻棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )
将由FeSO4、Ba(OH)2、AlCl3三种固体组成的混合物溶于足量的水中,用玻棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )
A.AB段发生反应的的离子方程式为:
Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O
B.C点表示的沉淀的化学式为Al(OH)3、BaSO4、Fe(OH)2
C.D点表示的溶液呈酸性
D.混合物中FeSO4和AlCl3的物质的量相等
查看答案和解析>>
科目: 来源: 题型:
隔绝空气,将20.8g铁、镁、铝混合物放入一定量硝酸中充分反应,当金属完全溶解,消耗硝酸amol,收集到bmolNO和cmolNO2的混合气体共8.96L(标准状况下,忽略N2O4),向反应后的溶液中加入适量的烧碱溶液,使沉淀量达到最大,过滤、洗涤、干燥、灼烧后,剩余固体质量为25.6g,则a:b:c为
A.10:1:2 B.5:1:2 C.10:1:3 D.无法计算
查看答案和解析>>
科目: 来源: 题型:
已建立化学平衡的某可逆反应,当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的质量分数一定增加 ②生成物产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速度一定大于逆反应速度 ⑥一定使用催化剂
A.①②③ B.②③⑤ C.④⑤⑥ D.②⑤
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.1molC10H20分子中,含29×6.02×1023个共用电子对
B.10mL18.4mol·L-1的浓硫酸与90mL蒸馏水混合,所得溶液中c(H+)=3.68 mol·L-1
C.25℃时,在pH=4的HCl溶液与pH=10的Na2CO3溶液中,由于HCl抑制水的电离、Na2CO3促进水的电离,溶液中c(H+)后者大于前者
D.在25mL0.1mol·L-1NaOH溶液中,滴入0.1 mol·L-1的CH3COOH溶液至混合溶液pH=7时,则滴加CH3COOH溶液的体积大于25mL
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,四种元素原子的最外层电子数之和为19,X和Y元素原子序数比6:7,X的最高正价是W是最低负价的绝对值的两倍。下列说法正确的是
A.X单质可以通过铝热法获得
B.Y的氧化物是良好的半导体材料
C.Z的氢化物比W的氢化物更稳定
D.X的最高价氧化物和Z的最高价氧化物化合的产物中有共价键和离子键
查看答案和解析>>
科目: 来源: 题型:
 X、Y、Z、W有如右图所示的转化关系,已知反应热:△H=△H1+△H2, 则X、Y不可能是
X、Y、Z、W有如右图所示的转化关系,已知反应热:△H=△H1+△H2, 则X、Y不可能是
A.C、CO
B.AlCl3 、Al(OH)3
C.Fe 、Fe(NO3)2
D.S、SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com