
科目: 来源: 题型:
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH = _______________![]() _.
_.
(2)反应Cl2+Na2SO3+2 NaOH===2NaCl+Na2SO4+H2O中的还原剂为________________.
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl![]() 、OH
、OH![]() 和SO
和SO![]() .请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
① 提出合理假设 .
假设1:只存在SO32-;假设2:既不存在SO32-也不存在ClO![]() ;假设3:_____________.
;假设3:_____________.
② 设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL![]() L-1H2SO4、1moL
L-1H2SO4、1moL![]() L-1NaOH、0.01mol
L-1NaOH、0.01mol![]() L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3 moL |
|
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
科目: 来源: 题型:
碳酸锂广泛应用于陶瓷和医药等领域。已![]() -锂辉石(主要成分为Li2O
-锂辉石(主要成分为Li2O![]() Al2O3
Al2O3![]() 4SiO2)为原材料制备Li2CO3的工艺流程如下:
4SiO2)为原材料制备Li2CO3的工艺流程如下:
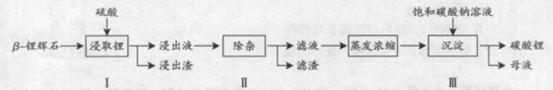
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g.
(1)步骤Ⅰ前,B-锂辉石要粉碎成细颗粒的目的是_____________.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、F![]() e2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钠”或“稀硫酸”)以调节溶液的PH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
e2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钠”或“稀硫酸”)以调节溶液的PH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有______________.
(4)步骤Ⅲ中,生成沉淀的离子方程式为________________.
(5)从母液中可回收的主要物质是_____________.
查看答案和解析>>
科目: 来源: 题型:
硼酸(H3BO3)在食品、医药领域应用广泛.
(1) 请完成B2H6气体与水反应的化学方程式:B2H6 + 6H2O=2H3BO3 +________.
(2) 在其他条件相同时,反应H3BO3 +3CH3OH![]() B(OCH3)3 +3H2O中,H3BO 3的转化率(
B(OCH3)3 +3H2O中,H3BO 3的转化率(![]() )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
① 温度对应该反应的反应速率和平衡移动的影响是_______.
② 该反应的![]() _____0(填“<”、“=”或“>”).
_____0(填“<”、“=”或“>”).
(3) H3BO 3溶液中存在如下反应:
H3BO 3(aq)+H2O(l)![]() [B(OH)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于29
[B(OH)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于29![]() 8K达到平衡时,c平衡(H+)=2. 0 × 10-5mol·L-1,c平衡(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字).
8K达到平衡时,c平衡(H+)=2. 0 × 10-5mol·L-1,c平衡(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字).
查看答案和解析>>
科目: 来源: 题型:
固定和利用CO2能有效地利用资源,并减少空气中的温室气体.CO2与化合物Ⅰ反应生成化合物Ⅱ,与化合物Ⅲ反应生成化合物Ⅳ,如反应①和②所示(其他试剂、产物及反应条件均省略).
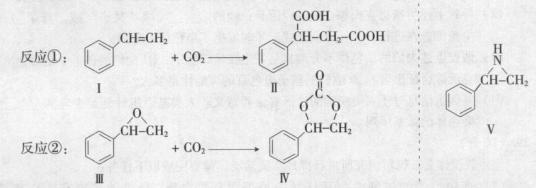
(1)化合物Ⅰ的分子式为______,1 mol该物质完全燃烧需消耗_______mol O2 .
(2)由![]() 通过消去反应制备Ⅰ的化学方程式为________(注明反应条件).。
通过消去反应制备Ⅰ的化学方程式为________(注明反应条件).。
(3)Ⅱ与过量![]() C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为________.
C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为________.
(4)在一定条件下,化合物V能与CO2发生类似反应②的反应,生成两种化合物(互为同分异构体),请写出其中任意一种化合物的结构简式:________.
(5)与CO2类似,CO也能被固定和利用.在一定条件下,CO、![]() 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应.下列关于Ⅵ和Ⅶ的说法正确的有________(双选,填字母).
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应.下列关于Ⅵ和Ⅶ的说法正确的有________(双选,填字母).
A.都属于芳香烃衍生物 B.都能使溴的四氯化碳溶液褪色
C.都能与Na反应放出H2 D. 1 molⅥ或Ⅶ最多能与4 mol H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
HA为酸性略强与醋酸的一元弱酸.在0.1mol.![]() NaA溶液中,离子浓度关系正确的是
NaA溶液中,离子浓度关系正确的是
A. c(![]() )
)![]() c(
c(![]() )
)![]() c(
c(![]() )
)![]() c(
c(![]() )
)
B. c(![]() )
)![]() c(
c(![]() )
) ![]() c(
c(![]() )
) ![]() c(
c(![]() )
)
C. c(![]() )+ c(
)+ c(![]() )= c(
)= c(![]() )+ c(
)+ c(![]() )
)
D. c(![]() )+ c(
)+ c(![]() )= c(
)= c(![]() )+ c(
)+ c(![]() )
)
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.乙烯和乙烷都能发生加聚反应
B.蛋白质水解的最终产物是多肽
C.米酒变酸的过程涉及了氧化反应
D.石油裂解和油脂皂化都有高分子生成小分子的过程
查看答案和解析>>
科目: 来源: 题型:
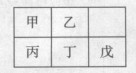
短周期金属元素甲~戊在元素周期表中的相对位置如右表所示:
下面判断正确的是
A.原子半径: 丙![]() 丁
丁![]() 戊 B金属性:甲
戊 B金属性:甲![]() 丙
丙
C.氢氧化物碱性:丙![]() 丁
丁![]() 戊 D.最外层电子数:甲
戊 D.最外层电子数:甲![]() 乙
乙
查看答案和解析>>
科目: 来源: 题型:
设 ![]() 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
A.16g ![]() 中含有4
中含有4![]() 个C-H键
个C-H键
B.1mol.![]()
![]() 溶液含有
溶液含有![]() 个
个![]()
C.1mol Cu和足量稀硝酸反应产生 ![]() 个NO分子
个NO分子
D.常温常压下,22.4L![]() 中含有
中含有 ![]() 个
个![]() 分子
分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com