
科目: 来源: 题型:
SnO2与Na2CO3、S共熔可转变为可溶性盐,反应方程式为:
SnO2+2Na2CO3+4S![]() Na2SnS3+Na2SO4+2CO2↑。下列说法正确的是
Na2SnS3+Na2SO4+2CO2↑。下列说法正确的是
A.高温条件下SnO2的氧化性强于S B.Na2SnS3是SnO2被氧化后的产物
C.生成1mol Na2SnS3时转移6mol电子 D.还原剂与氧化剂的质量比为3∶1
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是
A.根据沸点差异可以判断两种液体混合物是否可用蒸馏方法进行分离
B.根据固体溶解度曲线可以判断物质结晶的方法
C.根据熵变可以判断所有化学反应能否自发进行
D.根据化学平衡常数可以判断化学反应进行的限度
查看答案和解析>>
科目: 来源: 题型:
(1) 组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链。它完全燃烧时所消耗O2的体
积是同状况下该烃蒸气体积的8.5倍,由此分析回答:
①若该烃为链状二烯烃,并且与等物质的量的Br2加成后只能得到单一产物,请写出化学反应方程式: (有机物用结构简式表示)。
②若该烃只能与等物质的量的Br2发生加成反应,则其结构简式为 (填任一种)。
(2) 有机物A由于其特殊的结构,一直受到理论化学家的注意,由于缺乏有效的合成途径,一度
延缓对它的研究,直到1993年出现了可以大量制备的方法,才得以被重视。A是非极性分子,
化学式是C6H8,分子的核磁共振氢谱图显示只有一个吸收峰。
①A的结构简式为 ;A分子中在同一平面上的碳原子数为 。
②A的二氯取代产物的异构体有 种。
查看答案和解析>>
科目: 来源: 题型:
卤代烃(RX)可以合成格氏试剂(RMgX),合成格氏试剂及格氏试剂有关应用如下:(R为烃基,R1、R2为烃基或氢原子)
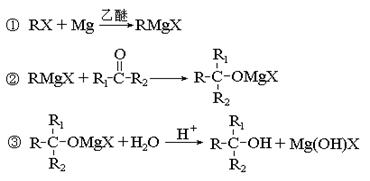
请回答下列问题:
⑴如上反应②的类型是 。
⑵CH3CH2MgCl与CO2在酸性水溶液中反应可生成有机物X,则X的结构简式为: 。
⑶![]() 与丙酮(CH3COCH3)在酸性水溶液中反应可生成有机物Y,有机物Y的同分异构体很多,其中属于酚类且苯环上除酚羟基外只有一个取代基的同分异构体共有 种。
与丙酮(CH3COCH3)在酸性水溶液中反应可生成有机物Y,有机物Y的同分异构体很多,其中属于酚类且苯环上除酚羟基外只有一个取代基的同分异构体共有 种。
⑷由正丙醇合成正丁醇的合成路线如下:
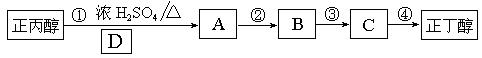
请回答下列问题:
①D的化学式 。
②写出与正丁醇互为同分异构体且在一定条件下能被CuO氧化,氧化产物能发生银镜反应的物质的结构简式: 。
![]() ③写出B C的化学方程式:
③写出B C的化学方程式:
查看答案和解析>>
科目: 来源: 题型:阅读理解
人类利用太阳能已有3000多年的历史,太阳能科技突飞猛进。塑晶学名为新戊二醇(NPG),它和液晶相似,塑晶在恒温44℃时,白天吸收太阳能而贮存热能,晚上则放出白天贮存的热能。NPG是一种白色结晶固体,熔点124-130℃,沸点210℃,主要作为生产聚酯树脂、无油醇酸树脂等。已知:NPG的结构式为:![]() ,试回答下列问题:
,试回答下列问题:
(1)有关NPG说法正确的是 (填序号)。
A.NPG与乙二醇互为同系物
B.NPG可命名为:2,2-二甲基-1,3-丙二醇
C. NPG一定条件下能发生消去反应
D.研究确定NPG的结构,需经重结晶提纯并干燥、元素定量分析确定分子、相对分子质量测定和波谱分析确定结构
(2)已知同一个碳原子连两个羟基该物质不稳定,与NPG互为同分异构体且属于5碳直链稳定的二元醇有: 种;在其所有异构体中,消去2个水分子得到橡胶单体异戊二烯(![]() )的二元醇结构可能有: 种。
)的二元醇结构可能有: 种。
(3)NPG可与丙二酸等物质的量缩聚形成一种用途非常广泛的聚酯,该反应的化学方程式为: 。
(4)NPG合成方法之一是利用两种醛加成后再用Cu-ZnO作催化剂加氢得到,已知:

则两种醛的结构简式是: 。
(5)二溴新戊二醇![]() ,是一种纤维类织品的阻燃剂,文献记载二溴新戊二醇的合成方法,“季戊四醇先与浓度在98%以上的醋酸进行酯化反应,再通入溴化氢气体进行取代反应,保温后分离出二溴新戊二醇的二酯化物,然后于0.4-0.6Mpa压力下用甲醇和无机酸进行恒压酯分解,该合成方法反应温度低,生成的粗品二溴新戊二醇含量可达88%左右,产品收率高。”
,是一种纤维类织品的阻燃剂,文献记载二溴新戊二醇的合成方法,“季戊四醇先与浓度在98%以上的醋酸进行酯化反应,再通入溴化氢气体进行取代反应,保温后分离出二溴新戊二醇的二酯化物,然后于0.4-0.6Mpa压力下用甲醇和无机酸进行恒压酯分解,该合成方法反应温度低,生成的粗品二溴新戊二醇含量可达88%左右,产品收率高。”
试补充合成路线(只写相关反应物和相关生成物)
 →□→□→
→□→□→![]()
查看答案和解析>>
科目: 来源: 题型:
(分)现有某金属的硝酸盐2.160g,充分加热分解生成金属氧化物0.960g和NO2、O2的混合气体0.0270mol(不考虑N2O4).请填空:
(1)混合气体中NO2的物质的量为________mol.
(2)将此组成的混合气体通入足量水中,剩余气体在标准状况下体积为________mL.
(3)该反应中金属元素的化合价________(填升高、降低、不变).
(4)写出该硝酸盐分解的化学方程式,标明电子转移的方向和数目.
查看答案和解析>>
科目: 来源: 题型:
工业生产粗硅的主要原理为:SiO2+2C 3273K Si(粗)+2CO↑。
(1)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为 ?? 。
(2)工业上可通过如下流程由粗硅制取纯硅:
| ||||||
|
| |||||
![]()
![]()
![]() Si(粗) SiCl4(l) Si(纯)
Si(粗) SiCl4(l) Si(纯)
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8t纯硅需纯度为75%的石英砂多少吨?
(3)工业上还可以通过下图所示的流程来制取纯硅:
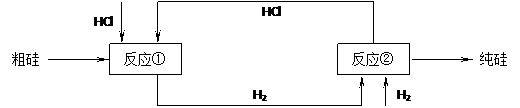
反应①: Si(粗)+3HCl(g) 553~573K SiHCl3(l)+H2(g)
反应②: SiHCl3+H2 1373K Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?
查看答案和解析>>
科目: 来源: 题型:阅读理解
(A)(10分)HN3称为叠氮酸,常温下为无色有刺激性气味的液体。N3—也被称为类卤离子。用酸与
 叠氮化钠反应可制得叠氮酸。而叠氮化钠可从下列反应制得:
叠氮化钠反应可制得叠氮酸。而叠氮化钠可从下列反应制得:
NaNH2+N2O=NaN3+H2O。HN3、浓盐酸混合液可溶解铜、铂、金等不活泼
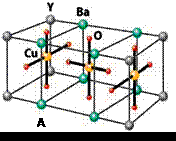
金属,如溶解铜生成CuCl2—。铜和铂的化合物在超导和医药上有重要应用,
Cu的化合物A(晶胞如图)即为超导氧化物之一,而化学式为Pt(NH3)2Cl2
的化合物有两种异构体,其中B异构体具有可溶性,可用于治疗癌症。试
回答下列问题:
(1)基态氮原子核外电子排布的轨道表示式为 。
(2)元素N、S、P的第一电离能(I1)由大到小的顺序为 。
(3)HN3属于 晶体,N3—的空间构型是_____,与N3—互为等电子体的分子的化学式为 (写1种)。NH2—的电子式为 ,其中心原子的杂化类型是 。
(4)CuCl2—中的键型为 ,超导氧化物A的化学式为
(5)治癌药物B的结构简式为
(B)(10分)以下是以绿矾、碳酸氢铵和氯化钾为原料制备生产市场较紧俏的硫酸钾产品的新工艺 。已知:反应(Ⅰ)的化学方程式为:FeSO4??7H2O+2NH4HCO3= FeCO3↓+(NH4)2SO4+CO2↑+H2O
反应(Ⅱ)的化学方程式为:(NH4)2SO4+2KC1=K2SO4+ 2NH4Cl
工艺流程如下:
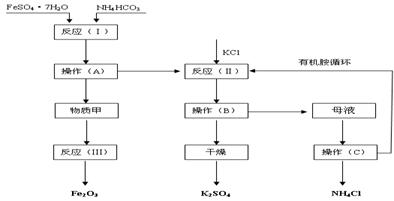
试回答下列问题:
(1)该工艺中的副产品是 。(填化学式)
(2)操作C的名称为 。
(3)原料绿矾、碳酸氢铵的最佳投料比是 (质量比)时,FeSO4的转化率大于95%。
(4)物质甲是 (填化学式),反应(Ⅲ)是甲物质与适量空气煅烧,温度为700~800℃,煅烧时间为1~1.5 h时可获得符合国标一级品要求的氧化铁红,其化学方程式是__________。
查看答案和解析>>
科目: 来源: 题型:
雷达的微波过滤器里使用铁氧磁性体,如钇铁石榴石Y3Fe5O12,其中Y是ⅢB族稀土元素。下面有关钇铁石榴石的叙述中正确的是
A.可表示为3YO3·3FeO·Fe2O3 B.可表示为Y3O5·Fe3O4·Fe2O3
C.其中钇、铁的化合价均为+3价 D.其中钇、铁的化合价均有+2、+3价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com