
科目: 来源: 题型:
钾钠合金(含50%—80%钾)可用作原子反应堆的导热剂,以下所述该合金的事实跟此项应用无关的是( )
A.熔点260.7 K B.具有很高的比热
C.可作冷却剂 D.能跟水剧烈反应
查看答案和解析>>
科目: 来源: 题型:
下列物质递变关系不正确的是( )?
A. 粒子半径:K>Na>Na+>Li+
B. 单质的密度:Li<K<Na<Rb?
C. 单质的还原性:Li>Na>K>Rb?
D. 跟水反应的剧烈程度:Li>Na>K>Rb
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式中正确的是
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应
CH3OH+H2O-6e-= CO2↑+6H+
B.在NaHSO4溶液中加Ba(OH)2至中性
H++SO42-+Ba2++OH-= BaSO4↓+H2O
C.苯酚钠的水溶液中通入少量的CO2
2C6H5O¯+CO2+H2O→2C6H5OH+CO32-
D.用侯氏制碱法制得NaHCO3
Na++NH3+CO2+H2O = NaHCO3↓+NH4+
查看答案和解析>>
科目: 来源: 题型:
合成氨反应N2(g)+3H2(g)![]() 2NH3(g)在某温度下达平衡时,各物质的浓度是c(N2)=3mol·L-1,c(H2)=9mol·L-1,c(NH3)=4mol·L-1,求该温度时的平衡常数和N2、H2的起始浓度。
2NH3(g)在某温度下达平衡时,各物质的浓度是c(N2)=3mol·L-1,c(H2)=9mol·L-1,c(NH3)=4mol·L-1,求该温度时的平衡常数和N2、H2的起始浓度。
查看答案和解析>>
科目: 来源: 题型:
在相同温度下,下列3个反应放出的热量分别以Q1、Q2、Q3表示,则Q1、Q2、Q3的关系是( )?
(1)2H2(g)+O2(g)![]() 2H2O(g) ΔH =Q1??
2H2O(g) ΔH =Q1??
(2)2H2(g)+O2(g)![]() 2H2O(l) ΔH =Q2?
2H2O(l) ΔH =Q2?
(3)H2(g)+1/2O2(g)![]() H2O(g) ΔH =Q3?
H2O(g) ΔH =Q3?
A.Q1>Q2,Q2=2Q3 B.Q1=Q2=Q3??
C.Q1>Q2,Q3=1/2Q1 D.无法比较?
查看答案和解析>>
科目: 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义,对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
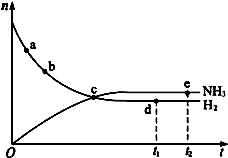
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大
查看答案和解析>>
科目: 来源: 题型:
写出下列制取氯气的化学反应方程式:
(1)实验室用二氧化锰跟浓盐酸反应制取氯气的化学反应方程式为_____________________。
(2)高锰酸钾(KMnO4)是常用的氧化剂,在酸性条件下,![]() 被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
(3)历史上曾用“地康法”制取氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中氧气跟氯化氢反应制取氯气,化学反应方程式为__________________________。
从氯元素化合价的变化来看,以上三种方法的共同点是____________,比较以上三个反应,可得出三种氧化剂的氧化能力由强到弱的顺序为____________。
查看答案和解析>>
科目: 来源: 题型:
已知某温度、压强下的气体摩尔体积为55.20 L·mol-1,在该条件下有1 mol气体X发生如下反应并达到平衡:2X(g)![]() mY(g)+Z(g),测得混合气体中X的体积分数为55.80%,混合气体的总质量为46.00 g,混合气体的密度为0.72 g·L-1。则平衡混合气体的平均相对分子质量为( )
mY(g)+Z(g),测得混合气体中X的体积分数为55.80%,混合气体的总质量为46.00 g,混合气体的密度为0.72 g·L-1。则平衡混合气体的平均相对分子质量为( )
A.58.80 B.46.00 C.39.74 D.16.13
查看答案和解析>>
科目: 来源: 题型:
下列化合物中,既显酸性又能发生加成反应的是( )
A、CH2=CH—CH2OH B、CH3COOH
C、CH2=CH—COOC2H5 D、CH2=CH—COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com