
科目: 来源: 题型:
周期表前20号元素中有A、B、C、D、E五种元素。已知它们都不是稀有气体元素,且原子半径依次减小,其中A和E同族,A与C、B与E原子的电子层数都相差2,A、B原子最外层电子数之比为1∶4。
(1)写出元素符号:B_____________,D_____________,E_____________。
(2)A和C能以原子数1∶1形成一种化合物,写出该化合物的化学式:_____________。
查看答案和解析>>
科目: 来源: 题型:
下列有关物质性质的比较中,正确的是( )
A.熔点:CO2<H2O<SiO2<KCl
B.粒子半径:K+>Na+>Mg2+>Al3+
C.酸性:H3PO4>H2SO4>HClO4>H2SiO3
D.稳定性:H2O<NH3<PH3<SiH4
查看答案和解析>>
科目: 来源: 题型:
家用液化气中的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出丁烷燃烧反应的热化学方程式:________________________。已知1 mol 液态水汽化时需要吸收44 kJ的热量,则1 mol 丁烷完全燃烧并生成气态水时放出的热量为______kJ。
查看答案和解析>>
科目: 来源: 题型:
一定温度下,当2mol的SO2和1mol的O2在体积一定的密闭容器中反应达到化学平衡状态时,下列叙述为该化学反应的限度最大的是( )
A.SO2的转化率为80% B.O2的转化率为80%
C.平衡时SO2的物质的量为0.5 mol D.平衡时O2的物质的量为0.6 mol
查看答案和解析>>
科目: 来源: 题型:
下列有关铝的说法正确的是
A.金属铝与盐酸或氢氧化钠溶液分别反应均产生0.2 mol氢气时,失去的电子数不同
B.铝既能与盐酸反应(生成AlCl3),又能与NaOH溶液反应(生成NaAlO2),所以金属铝具有两性
C.金属铝能在空气中形成一层致密的氧化膜,因此是一种比较活泼的金属,所以将少量铝投入到过量的FeCl3溶液中,可以置换出金属铁
D.铝元素在人体内聚集过多,对健康不利,建议尽量少用铝制餐具、铝制食品包装袋、铝制易拉罐等
查看答案和解析>>
科目: 来源: 题型:
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要。下列关于天然气水合物中两种分子极性的描述正确的是( )
A.两种都是极性分子 B.两种都是非极性分子
C.CH4是极性分子,H2O是非极性分子 D.H2O是极性分子,CH4是非极性分子
查看答案和解析>>
科目: 来源: 题型:
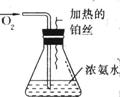 按图所表示的装置进行实验:
按图所表示的装置进行实验:
(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐_________.有关化学方程式为________________
(2)由于气温的原因,上述实验一段时间后现象不太明显,应该向锥形瓶内加入下列哪种物质才能看到明显的现象________(填字母)。
A.NaOH固体 B.生石灰 C.浓H2SO4 D.NH4Cl固体
(3)经过对比试验证明。在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是 __________________
查看答案和解析>>
科目: 来源: 题型:
常温下,将氨水与盐酸溶液以任意比例混合,充分反应后,溶液中离子浓度的大小关系可能为( ).
①c(NH4+)>c(Cl-)>c(OH-)>c(H+)②c(Cl-)>c(NH4+)>c(H+)>c(OH-)③c(NH4+)>c(OH-)>c(Cl-)>c(H+)④c(NH4+)=c(Cl-)>c(OH-)=c(H+)⑤c(Cl-)>c(H+)>c(NH4+)>c(OH-)
A只有①④ B只有②④
C只有①②④ D①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
为抵制全球金融风暴,我国计划在未来三年内投资4万亿资金拉动内需,但“科学发展”和拉动内需紧密结合才能产生长远的社会和经济效益。下列说法正确的是( )
![]() A.工业发展需要大量煤炭,故应大量开采煤炭满足生产要求
A.工业发展需要大量煤炭,故应大量开采煤炭满足生产要求
![]() B.大气中氯氟烃的减少带来的积极效果是减缓臭氧空洞的增大
B.大气中氯氟烃的减少带来的积极效果是减缓臭氧空洞的增大
![]() C.1mol S完全燃烧最终全部转化成稳定化合物时电子转移4mol
C.1mol S完全燃烧最终全部转化成稳定化合物时电子转移4mol
![]() D.工业生产中排放的废渣、废水、废气只能对环境产生影响,无任何价值
D.工业生产中排放的废渣、废水、废气只能对环境产生影响,无任何价值
查看答案和解析>>
科目: 来源: 题型:
托盘天平两盘内的小烧杯中,分别盛有足量的稀硫酸,此时天平平衡。向两烧杯中分别加入0.1 mol两种金属中的各一种,充分反应后,天平仍保持平衡,则两种金属应分别是
A.Mg和A1 B.Fe和A1 C.Mg和Na D.Fe和Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com