
科目: 来源: 题型:
在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+![]() O2(g)====CO2(g)+2H2O(l);ΔH=+725.8 kJ·mol-1
O2(g)====CO2(g)+2H2O(l);ΔH=+725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=-1 452 kJ·mol-1
C.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=+1 452 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知反应X+Y====M+N为放热反应,对该反应的下列说法中正确的是( )
A.X的能量一定高于M
B.Y的能量一定高于N
C.X和Y的总能量一定高于M和N的总能量
D.因该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目: 来源: 题型:
在氯化铁与氯化铜的混合溶液中加入过量的铁粉,搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则原溶液中FeCl3和CuCl2物质的量之比为( )
A.2∶7 B.7∶2
C.5∶2 D.2∶5
查看答案和解析>>
科目: 来源: 题型:
R元素的质量数为A,Rn-的核外电子数为x。则W g Rn-所含中子的物质的量为( )
A.(A-x+n) mol B.(A-x-n) mol
C.![]() (A-x+n) mol D.
(A-x+n) mol D.![]() (A-x-n) mol
(A-x-n) mol
查看答案和解析>>
科目: 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与B形成离子化合物A2B,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试完成下列问题:
(1)写出五种元素的元素符号:A__________,B__________,C__________,D__________,E__________。
(2)用电子式表示离子化合物A2B的形式过程:____________________________。
(3)写出下列物质的电子式:
①D元素形成的单质____________________;
②E与C形成的化合物____________________;
③A、B、E形成的化合物____________________;
④D与E形成的化合物____________________。
查看答案和解析>>
科目: 来源: 题型:
B环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)★ | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)★ | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7 溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应
增多。实验中将酸性Na2Cr2O7 溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7 溶液的加料方式为 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水MgSO4 固体,除去有机物中的少量水。
①上述操作的正确顺序是 (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 。
③在上述操作c中,加入NaCl 固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学
环境的氢原子。
查看答案和解析>>
科目: 来源: 题型:
有6瓶白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、硫酸铵、无水硫酸铜、碳酸钠,现只提供蒸馏水,通过下面的实验步骤即可鉴别它们。请完成下列问题:
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是__________________________________,被检出的物质的化学式(分子式)是_____________。
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象是1支试管中有白色沉淀生成,写出相应反应的离子方程式(下同):____________________,2支试管中有蓝色沉淀生成:_______________________,被检出的物质的化学式(分子式)是_____________。
(3)鉴别余下未检出物质的方法和观察到的现象是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
在鲜活鱼的长途运输中,必须考虑以下几点:水中需要保持适量的O2,及时除去鱼排出的CO2;防止细菌的大量繁殖.现有两种在水中能起供氧灭菌作用的物质,其性能如下:
过氧化钠(Na2O2):易溶于水,与水反应生成NaOH和O2;?
过氧化钙(CaO2):微溶于水,与水反应生成Ca(OH)2(微溶)和O2。
根据以上介绍,你认为运输鲜活水产品时应选择 加入水中,原因是 。
查看答案和解析>>
科目: 来源: 题型:
某地有一池塘,生长着丰富的水生植物和多种鱼虾。后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡。根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了 。
(2)造成这种变化的原因是 。
(3)经检测,污水中含有0.012 mol·L-1的游离溴。可用亚硫酸钠除去污水中的溴,请写出其化学方程式 。
(4)处理这种污水5 L,需加入0.05 mol·L-1的亚硫酸钠__________L,才能将溴全部除去。
(5)要使池塘恢复本来面目.首先要解决的问题是__________.首先要恢复的生物是__________。
查看答案和解析>>
科目: 来源: 题型:
某课外活动小组设计了如图所示(夹持装置已略去)的一套装置,用H2和CuO冶炼Cu。准确称取3.180 g CuO放在硬质玻璃管内.已知:CuO—黑色、Cu2O—红色、Cu—红色。
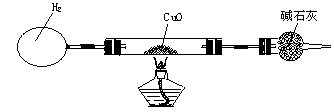
试通过计算回答[①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00]:
(1)下列H2球较适合用于本实验的是__________(填选项编号)
A.500 mL H2 球 B.896 mL H2 球 C.1500 mL H2 球
(2)反应至黑色全部变为红色止,测量H2球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g。则:
①参加反应的H2的质量为:__________;
②假设红色物质为单一物质,则红色物质的化学式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com