
科目: 来源: 题型:
将5.6g铁放入含有x mol FeCl3和y molCuCl2的混合溶液中,充分反应后,固体粉末仍为5.6g。则x: y可能是( )
A.3:7 B.8:7 C.1:7 D.1:1
查看答案和解析>>
科目: 来源: 题型:
下列各组离子,一定能大量共存的是
A.常温下,c(H+)/c(OH-)=1×10-12的溶液:I-、Cl-、HCO3-、Na+
B.含有大量Fe3+的溶液:Na+、HCO3-、NO3-、CO32-
C.加入铝粉能产生氢气的溶液:Cl-![]() 、Na+、SO42-、NO3-
、Na+、SO42-、NO3-
D.由水电离出的c(H+)=1×10-12 mol??L-1溶液中:K+、Cl- 、NO3- 、Na+
查看答案和解析>>
科目: 来源: 题型:
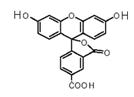 2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质,5-羧基荧光素(5-FAM)
2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质,5-羧基荧光素(5-FAM)
结构简式如右图所示,在碱性条件下有强烈的绿色荧光,广泛
应用于荧光分析等。下列有关5-FAM说法不正确的是
A.可与碳酸氢钠溶液反应
B.分子式为C21H12O7
C.1mol 该物质与足量NaOH溶液反应,可消耗4 mol氢氧化钠
D.不与FeCl3发生反应
查看答案和解析>>
科目: 来源: 题型:
利用化学原理可以对工厂排放的废水进行有效检测和合理处理。
(1)染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润红色石蕊试纸变蓝的气体)。除去NO2-离子的离子方程式是
▲ 。
(2)废水中的N、P元素是造成水体富营养化的主要因素,农药厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过两种方法将其除去。
①方法一:将Ca(OH)2或CaO投加到待处理的废水中,生成磷酸钙,从而进行回收。当处理后的废水中c(Ca2+)=2×10-7mol/L时,溶液中c(PO43-)= ▲
(已知常温时,KSP[Ca3(PO4)2]=2×10-33)
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石——鸟粪石,反应的方程式为Mg2++ NH4++ PO43-= MgNH4 PO4。该方法中需要控制污水的pH为7.5-10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能是 ▲ 。与方法一相比,方法二的优点是 ▲ 。
(3)三氯乙烯在印刷、纺织等行业应用广泛,为了减少其对环境的影响,可将三氯乙烯在二氧化钛薄膜上催化降解,其反应的机理如下:

该反应的总化学方程式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
阿斯匹林是一种常见的OTC药物,常用于治疗因感冒引起的头痛发热。阿斯匹林可按下列流程合成。

试回答:
(1)有机物C的结构简式为________________;
(2)以上反应中属于氧化反应的反应有②和__________(填编号);
(3)反应①的化学方程式为________________________________________;
(4)任写一种E的属于酯类的同分异构体________________。
查看答案和解析>>
科目: 来源: 题型:
设阿伏加德罗常数为NA,下列说法中正确的是
A.室温时,8 g甲烷气体所含的共价键数为2 NA
B.在标准状况下,11.2 L SO3所含的氧原子数为1.5 NA
C.32g氧气与金属钠反应生成过氧化钠时得到的电子数为4NA
D.1 L 2 mol/L 的MgCl2溶液中所含的Cl-数为2 NA
查看答案和解析>>
科目: 来源: 题型:
A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图17 (反应条件和部分产物略去)。试回答:

(1)E的电子式是 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是 。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是 。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+) 。
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是 。(已知甲醇的燃烧热![]() ,氢气的燃烧热
,氢气的燃烧热![]() )
)
查看答案和解析>>
科目: 来源: 题型:
胡锦涛同志在十七大报告中指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是( )
A.大量使用化学肥料,提高农作物的产量和质量
B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的液中加
0.1mol Cu(OH)2后恰好恢复到电解前的浓度和PH。则电解过程中转移的电子为
A、0.1mol B、0.2mol C、0.3mol D、0.4mol
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
![]() A.MgSO4晶体中只存在离子键
A.MgSO4晶体中只存在离子键
![]() B.含Ca2+、Mg2+的水都是硬水
B.含Ca2+、Mg2+的水都是硬水
![]() C.雾是气溶胶,在阳光下可观察到丁达尔效应
C.雾是气溶胶,在阳光下可观察到丁达尔效应
![]() D.玻璃是氧化物,成分可表示为
D.玻璃是氧化物,成分可表示为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com