
科目: 来源: 题型:
现有一瓶物质,为甲和乙的混合物,已知甲和乙的某些性质如下表,据此,将甲和乙分离的最佳方案是( )
| 物质 | 分子式 | 熔点 | 沸点 | 密度 | 可溶性 |
| 甲 | C3H6O2 | -98 ℃ | 57.5 ℃ | 0.93 | 溶于水 |
| 乙 | C4H8O2 | -84 ℃ | 77 ℃ | 0.91 | 溶于水 |
A.萃取法 B.升华法 C.分馏法 D.分液法
查看答案和解析>>
科目: 来源: 题型:
诺龙属于国际奥委会明确规定的违禁药物中的合成代谢类物质,其结构简式如右图所示,下列有关诺龙性质的说法中,正确的是( )
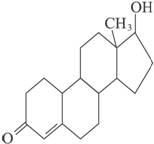
A.所有碳原子都在同一平面内
B.诺龙的分子式为C18H23O2
C.能发生取代、消去、加成、酯化、水解等反应
D.用新制的氢氧化铜悬浊液可将诺龙和乙醛鉴别开来
查看答案和解析>>
科目: 来源: 题型:
天然蛋白质水解产物中含化合物A,A由C、H、O、N四种元素组成,A能与NaOH反应,也能与盐酸反应,在一定条件下,两分子的A发生反应生成B和一个水分子,B的相对分子质量为312。此化合物遇浓硝酸显黄色,由上推断,A的结构简式为______________,
B的结构简式为______________________。
查看答案和解析>>
科目: 来源: 题型:
已知苯的同系物可被酸性KMnO4氧化,如:![]()
又知涤纶树脂的结构简式为: ?。工业上因苯二甲酸不易提纯,故用较易提纯的对苯二甲酸二甲酯和乙二醇为主要原料,按下列工艺流程合成涤纶树脂:
?。工业上因苯二甲酸不易提纯,故用较易提纯的对苯二甲酸二甲酯和乙二醇为主要原料,按下列工艺流程合成涤纶树脂:



试回答下列问题:
(1)用化学方程式表示上述工艺流程中各步转化过程。
(2)在合成涤纶树脂时,在缩聚的最后阶段要高温高真空,蒸出一种沸点较低的单体,请说明理由。
(3)现代工业以对苯二甲酸和乙二醇为单体合成涤纶树脂,在配料时若乙二醇和对苯二甲酸按物质的量101∶100配比,求合成的高聚物的平均相对分子质量最高能达到多少?
查看答案和解析>>
科目: 来源: 题型:
在下列反应中,盐酸作氧化剂的是( )
A.NaOH+HCl====NaCl+H2O B.CaCO3+2HCl====CaCl2+CO2↑+H2O
C.Zn+2HCl====ZnCl2+H2↑ D.MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
有一支50 mL酸式滴定管,其中盛有溶液,液面恰好在10.0 mL刻度处。将滴定管中的溶液全部流下排出,承接在量筒中,量筒内溶液的体积( )
A.大于40.0 Ml B.等于40.0 mL C.小于40.0 mL D.等于10.0 mL
查看答案和解析>>
科目: 来源: 题型:
下图曲线a表示放热反应X(g)+Y(g)![]() Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )

A.升高温度 B.加大X的投入量 C.加催化剂 D.增大体积
查看答案和解析>>
科目: 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+HC![]() CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH![]() CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC![]() CH(g ) △H2=32.4 kJ·mol-1
CH(g ) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g)=CH3CH![]() CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
查看答案和解析>>
科目: 来源: 题型:
下列反应按n(X)∶n(Y)=1∶2的比例在某压强下达到平衡:X(g)+2Y(g)![]() 2Z(g)(正反应为吸热反应)。已知X的转化率为20%时温度为100 ℃。如果温度提高一倍时转化率也增大一倍,平衡时当反应物总物质的量和生成物总物质的量相等时温度应为多少?
2Z(g)(正反应为吸热反应)。已知X的转化率为20%时温度为100 ℃。如果温度提高一倍时转化率也增大一倍,平衡时当反应物总物质的量和生成物总物质的量相等时温度应为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com